Abstract
In the last two decades, ionic liquids have been emerging as green materials and attracted much attention from scientists due to their broad application in many fields such as catalysis, electrochemistry, and biomass conversion. 1-Methylimidazolium hydrogen sulfate and 1-(4-sulfonic acid) butyl-3-methylimidazolium hydrogen sulfate ([MimC4SO3H]HSO4) were successfully prepared, and their chemical structures were elucidated by IR, HRMS. In this study, their catalytic activity was studied and compared with some inorganic catalysts through the preparation of fructose to 5- hydroxymethylfurfural (HMF) in the condition of stirring at room temperature. The result showed that among the tested catalysts for this reaction, [MimC4SO3H]HSO4 was the best one with a yield of 86% after 24 hours. In addition, this Brønsted acid catalyst could be reused five times without significant loss of catalytic activity. Base on previous literature and our results, the plausible mechanism of fructose dehydration into HMF was proposed in this study.
GIỚI THIỆU
5-Hydroxymethylfurfural (HMF), một hợp chất hữu cơ vòng furan quan trọng, chứa các nhóm định chức như carbonyl (aldehyde) và hydroxyl (alcohol) ở vị trí 2 và 5, để sản xuất nhiên liệu tái tạo 1 , 2 . HMF chủ yếu được sản xuất thông qua các phản ứng khử nước của đường (như glucose, fructose và sucrose) với các chất xúc tác đồng thể (thí dụ: sulfuric acid, chlohydric acid, aluminium chloride, chromium chloride) hoặc các chất xúc tác dị thể (thí dụ: zirconium oxide, zeolite, khung kim loại hữu cơ) trong hệ thống hai pha 3 , 4 , 5 , 6 , 7 , 8 . Xúc tác đồng thể Brønsted hoặc Lewis thường được sử dụng và là chất xúc tác hiệu quả cho quá trình này 9 . Tuy nhiên, các xúc tác này có một số nhược điểm như phải sử dụng một lượng lớn chất xúc tác, không thể thu hồi và tái sử dụng được, nguy hiểm khi thao tác (sulfuric acid gây bỏng da, hơi chlohydric acid gây suy hô hấp và tiêu hóa về lâu dài có thể ảnh hưởng đến thị giác) và ăn mòn thiết bị rất nhanh. Chất xúc tác acid dị thể mang lại những ưu điểm nổi bật như có thể thu hồi và tái chế dễ dàng, hứa hẹn là sự thay thế hiệu quả cho các chất xúc tác acid vô cơ 10 , tuy nhiên, chất xúc tác loại này cho hiệu suất phản ứng thấp do sự cạnh tranh của các phản ứng phụ, tạo ra sản phẩm phụ không mong muốn 11 . Chất lỏng ion (IL) đã được nghiên cứu rộng rãi cho phản ứng khử nước này. IL có khả năng phân hủy sinh học, không bay hơi, độc tính rất thấp và có hiệu quả cao do có khả năng gắn kết các nhóm chức đa dạng lên cation hoặc anion. Do đó, nhiều công trình nghiên cứu sử dụng IL làm chất xúc tác cũng như làm dung môi trong phản ứng khử nước fructose để tạo thành HMF 12 , 13 . Chất lỏng ion chứa imidazolium với Cl − có khả năng hòa tan đường cao nên 1-ethyl-3-methylimidazolium chloride ([EMIM]Cl) được sử dụng làm dung môi. Protic acid có thể xúc tác sự khử nước của fructose thành HMF, do đó, sự kết hợp của Cl − (để hòa tan đường) và cation proton của Brønsted acid (để xúc tác sự mất nước của fructose) được lựa chọn. Nghiên cứu này tiến hành khảo sát hiệu suất điều chế HMF từ fructose trong [EMIM]Cl với sự hiện diện của xúc tác Brønsted acid (acid vô cơ và chất lỏng chứa imidazolium cation). [MimC 4 SO 3 H]HSO 4 đã được chứng minh là chất xúc tác hiệu quả để khử fructose thành HMF trong [EMIM]Cl.
VẬT LIỆU VÀ PHƯƠNG PHÁP
Hóa chất
1,4-Butanesultone (Sigma Aldrich, 99,5%), diethyl ether (DE) (Fisher, 99,5+%), 1-methylimidazole (Sigma Aldrich, 99%), acid sulfuric (Merck, 95−97 %), phosphoric acid (Merck, 85 %), nitric acid (Merck, 65 %), chlorhydric acid (Merck, 37 %), [EMIM]Cl (Sigma-Aldrich, ≥95%), fructose (Sigma Aldrich, 99,0 %), ethyl acetate (EA) (Merck, ≥ 99,5%), HMF (Sigma Aldrich, 99 %), methanol (Merck, ≥ 99,9%).
Thiết bị
Phản ứng được thực hiện trên máy khuấy từ điều nhiệt IKA-RET. Xác định cấu trúc hóa học bằng phổ cộng hưởng từ hạt nhân với máy Bruker Avance II 500 MHz. Quang phổ hồng ngoại IR được ghi bằng máy Shimadzu IRPrestige-21 (KBr). Dữ liệu HRMS (ESI) được thu thập bằng Sciex X500R QTOF. Định lượng HMF trong quá trình khảo sát điều kiện phản ứng được thực hiện trên máy sắc ký lỏng hiệu năng cao Agilent Technologies 1260 Infinity đầu dò PDA (bước sóng 285 nm), cột sắc ký InertSustain C18 (5 µm; 4,6 x 150 mm), tốc độ dòng: 0,7 mL/phút, pha động gồm H 2 SO 4 2,5 mM (B) và methanol (A), chương trình pha động như sau: 0-2,5 phút, 100% B; 2,5-2,51 phút, 85% B; 2,51-17 phút, 85% B; 17-17,01 phút, 100 % B; 17,01-25 phút, 100 % B.
Nghiên cứu chưa đủ điều kiện để khảo sát sản phẩm phụ sinh ra trong quá trình phản ứng nên hiệu suất đề cập là hiệu suất HMF hình thành, được tính theo công thức sau
H% = (số mol HMF)/(số mol fructose ban đầu)x100%
Qui trình điều chế xúc tác14
Xúc tác 1-(4-sulfonic acid) butyl-3-methylimidazolium hydrogen sulfate ([MimC4SO3H]HSO4)
[MimC 4 SO 3 H]HSO 4 được điều chế theo sơ đồ được mô tả trong Figure 1 . Trong bình cầu 50 mL, 1,4-butanesultone (820 mg, 10 mmol) và 1-methylimidazole (1360 mg, 10 mmol) được khuấy trộn cùng nhau ở nhiệt độ 80 o C trong 12 giờ. Hỗn hợp sản phẩm màu trắng được rửa bằng diethyl ether (20 x 3 mL). Sau đó, thêm một lượng vừa đủ sulfuric acid (980 mg, 10 mmol) tiếp tục khuấy trong 6 giờ ở nhiệt độ 60 o C. Chất rắn được hòa tan hoàn toàn tạo thành sản phẩm thô, tiếp tục rửa bằng diethyl ether (20 x 3 mL) để thu [MimC 4 SO 3 H]HSO 4 tinh sạch.
Xúc tác 1- methylimidazolium hydrogen sulfate ([Mim]HSO4)
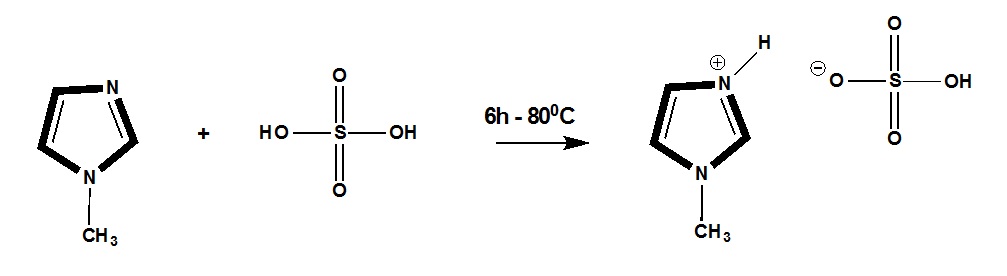
[Mim]HSO 4 được điều chế theo sơ đồ được mô tả trong Figure 2 . Trong bình cầu 50 mL, 1-methylimidazole (1360 mg, 10 mmol) được khuấy trộn cùng sulfuric acid (980 mg, 10 mmol) gia nhiệt ở 80 o C trong 6 giờ. Chất rắn được hòa tan hoàn toàn tạo thành sản phẩm thô, tiếp tục rửa bằng diethyl ether (20 x 3 mL). Kết quả tạo thành [Mim]HSO 4 .
Qui trình điều chế HMF
Dựa theo tài liệu công bố trước đây 15 , 16 , HMF được điều chế theo sơ đồ được mô tả trong Figure 3 . [EMIM]Cl được chọn làm dung môi cho phản ứng. Khảo sát số lượng hợp chất xúc tác IL điều chế được ở nhiệt độ phòng cho thấy với 20 mol% phản ứng tạo thành là HMF nhiều nhất. Với kết quả thu được, tiếp tục khảo sát hoạt tính của các xúc tác ở điều kiện như sau: 6 mmol [EMIM]Cl, 1 mmol fructose và 20 mol% hợp chất xúc tác được cho vào bình cầu đáy tròn 10 mL. Khuấy hỗn hợp phản ứng trong một khoảng thời gian ở nhiệt độ phòng ( Figure 4 ), trong đó thời gian được thay đổi để tối ưu hóa điều kiện phản ứng. Quá trình của phản ứng được theo dõi bằng sắc ký lỏng hiệu năng cao (HPLC). Việc tinh chế sản phẩm từ hỗn hợp phản ứng được thực hiện bằng phương pháp chiết lỏng-lỏng để thu được sản phẩm tinh sạch. Sản phẩm HMF được nhận danh cấu trúc hóa học bởi HRMS (ESI) và 1 H-NMR. Cơ chế phản ứng được đề nghị trong Figure 5 .
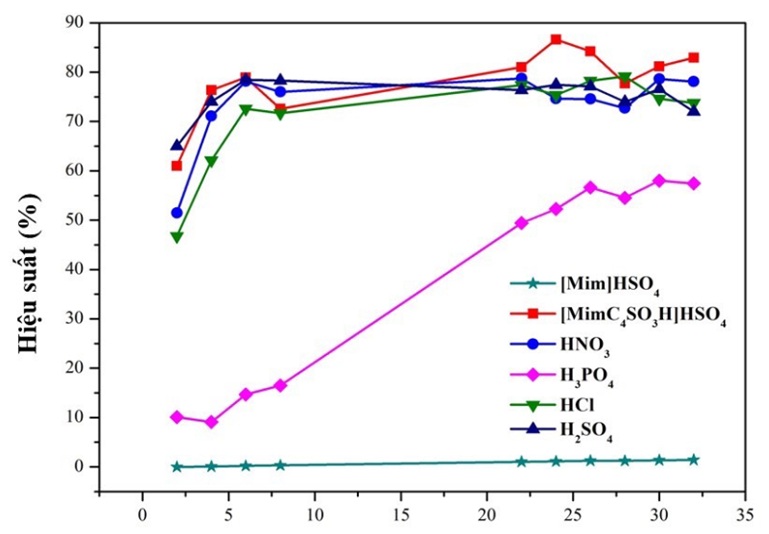
Figure 4 . Khảo sát thời gian phản ứng giữa fructose và xúc tác ở nhiệt độ phòng
1 H-NMR (500 MHz, CDCl 3 ): δ 9,58 (1H, s); 7,21 (1H, d, J = 3,2 Hz); 6,51 (1H, d, J = 3,2 Hz); 4,71 (2H, s).
HRMS (ESI) m/z 127,0379 [C 6 H 6 O 3 +H] + (tính toán lý thuyết cho C 6 H 6 O 3 +H là 127,0395).
KẾT QUẢ VÀ THẢO LUẬN
Xác định cấu trúc hóa học của hợp chất xúc tác
Xúc tác [Mim]HSO4
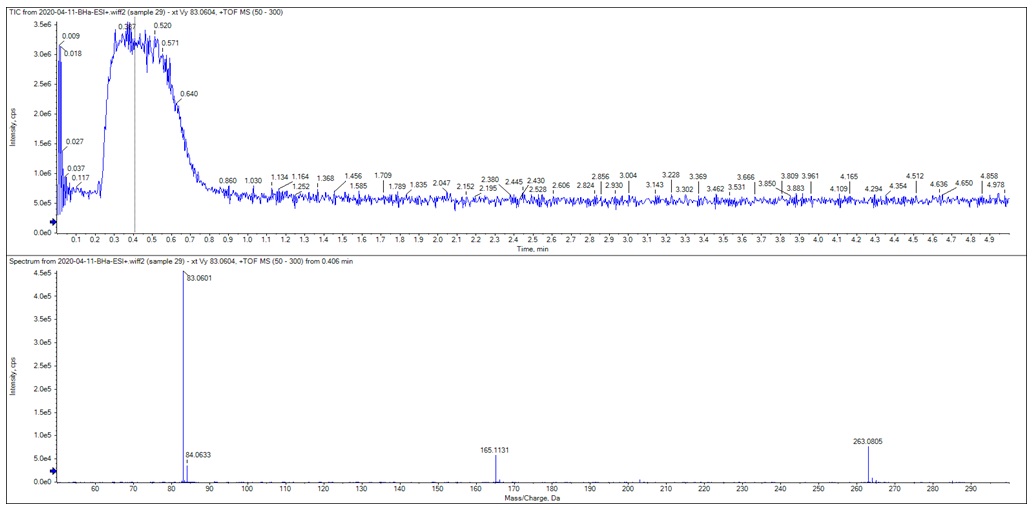
Khối phổ HRMS (ESI, positive) cho mũi ở m/z 83,0601 [Mim] + , tính toán lý thuyết [Mim] + là 83,0609 ( Figure 6 ).
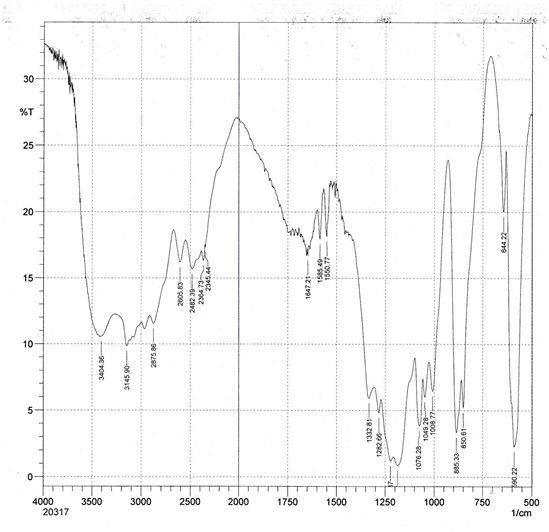
Phổ IR (KBr, 4000–500 cm -1 ) của [Mim]HSO 4 ( Figure 7 ) cho tín hiệu ở 3404 cm -1 là đặc trưng của liên kết O-H. Tín hiệu tại 3146 cm -1 dao động đặc trưng của liên kết N-H. 3078 cm -1 là dao động của nối H-C sp2 . Số sóng 2876 cm -1 , 1647 cm -1 là dao động của liên kết C sp3 -H, C=C. Số sóng 1585 cm -1 là dao động biến dạng của C sp2 -H. Tín hiệu tại 1186 cm -1 chứng tỏ có nối O=S=O ( Figure 7 ).
Xúc tác [MimC4SO3H]HSO4
Phổ HRMS (ESI, positive) Cho mũi ở m/z 219,0806 [MimC 4 SO 3 H] + , tính toán [MimC 4 SO 3 H] + là 219,0803 ( Figure 8 ).
Phổ IR (KBr, 4000–500 cm -1 ) của [MimC 4 SO 3 H]HSO 4 ( Figure 9 ) cho thấy mũi ở 3385 cm -1 là đặc trưng của dao động của liên kết O-H. Tín hiệu ở 3115 cm -1 là của dao động nối H-C sp2 . Tín hiệu đặc trưng của C sp3 -H ở 2962 cm -1 . Mũi ở 2361 cm -1 thể hiện dao động biến dạng của liên kết N-C. 1636 cm -1 là dao động của liên kết C=C, 1458 cm -1 là dao động biến dạng của C sp2 -H. Tín hiệu tại 1186 cm -1 chứng tỏ có nhóm chức O=S=O ( Figure 9 ).
Số liệu IR thu được của hai IL đều phù hợp với nghiên cứu của Ullah và cộng sự (2015) [14]. [Mim]HSO 4 : 3434,68; 2941,18; 2705,89; 2541,65; 1648,61; 1461,44; 1188,72; 1042,81; 850,30; 593,61 (cm -1 ). [MimC 4 SO 3 H]HSO 4 : 3451,08; 2945,73; 2716,49; 2541,31; 1640,91; 1452,04; 1192,52; 1048,34; 854,42 (cm -1 ).
Hoạt tính của xúc tác được nghiên cứu trên phản ứng tổng hợp HMF từ fructose.
Khảo sát điều kiện phản ứng
Kết quả khảo sát thời gian phản ứng tổng hợp HMF được trình bày ở Figure 4 . Hiệu suất phản ứng được khảo sát theo các mốc thời gian 2, 4, 6, 8, 22, 24, 26, 28, 30, 32 giờ thì nhận thấy H 3 PO 4 và [Mim]HSO 4 cho kết quả kém hơn so với các hợp chất xúc tác còn lại (theo dõi phản ứng bằng HPLC, Figure 10 ). Trong số các chất lỏng ion khảo sát, [Mim]HSO 4 là loại Brønsted acid dạng muối amonium nên cho hiệu suất phản ứng thấp nhất. Trong số các acid vô cơ khảo sát, H 3 PO 4 là acid phân ly ra ion H + ít nhất (pKa của H 3 PO 4 = 2,12; HCl = -8; H 2 SO 4 = -3 và HNO 3 = -1,3) 17 nên cho hiệu suất thấp. Các hợp chất xúc tác H 2 SO 4 , HCl, HNO 3 cho hiệu suất cao khoảng 78% sau 6 giờ. Sau 24 giờ, [MimC 4 SO 3 H]HSO 4 cho hiệu suất cao nhất là 86%. Sử dụng [MimC 4 SO 3 H]HSO 4 mặc dù thời gian dài hơn nhưng hiệu suất cao hơn. Ngoài ra, [MimC 4 SO 3 H]HSO 4 thân thiện với môi trường hơn các hợp chất xúc tác vô cơ. Chất lỏng ion [MimC 4 SO 3 H]HSO 4 cho hiệu suất cao hơn hẳn [Mim]HSO 4 , có thể giải thích do tâm xúc tác là cation SO 3 H [MimC 4 SO 3 H]HSO 4 , phần anion HSO 4 - không đóng góp nhiều trong phản ứng này. Xúc tác chất lỏng ion cho hiệu suất cao hơn do quá trình tiếp xúc pha và khuếch tán của chất lỏng ion trong hỗn hợp phản ứng tốt hơn các acid vô cơ. Cơ chế phản ứng chuyển hóa fructose thành HMF được mô tả trong Figure 5 .
Thu hồi và tái sử dụng chất xúc tác
Chất lỏng ion [MimC 4 SO 3 H]HSO 4 sau khi thực hiện phản ứng 24 giờ được thu hồi theo quy trình như sau: HMF hình thành sau phản ứng được chiết bằng dung dịch EA: DE (9: 1) (10 × 5 mL) theo dõi bằng sắc ký lớp mỏng (TLC) đến khi chiết hết HMF trong hỗn hợp phản ứng. Sau khi chiết hết HMF, cho 1 mmol fructose vào hỗn hợp còn lại sau khi chiết HMF để tiếp tục phản ứng ở cùng điều kiện. Hiệu suất phản ứng thay đổi không đáng kể sau 5 lần tái sử dụng ( Figure 11 ). Nghiên cứu trước đây cũng đã báo cáo về việc tái sử dụng xúc tác [MimC 4 SO 3 H]HSO 4 dễ dàng với hiệu suất không đổi 18 .
Figure 11 . Hiệu suất phản ứng qua các lần tái sử dụng xúc tác [MimC 4 SO 3 H]HSO 4
KẾT LUẬN
Hai chất lỏng ion đã được điều chế thành công theo quy trình đã được công bố. Cấu trúc hóa học của 2 chất lỏng ion cũng được xác định bằng phổ IR và HRMS (ESI). Hoạt tính của xúc tác được khảo sát thông qua phản ứng điều chế fructose thành HMF trong điều kiện khuấy ở nhiệt độ phòng trong 2−32 giờ. So với chất xúc tác vô cơ, xúc tác [MimC 4 SO 3 H]HSO 4 cho hiệu suất cao hơn và đặc biệt là thân thiện với môi trường hơn (an toàn khi sử dụng và xúc tác [MimC 4 SO 3 H]HSO 4 sau phản ứng được tái sử dụng một cách dễ dàng).
DANH MỤC CÁC TỪ VIẾT TẮT
IL: Chất lỏng ion.
[Mim]HSO 4: 1-Methylimidazolium hydrogen sulfate
[MimC 4 SO 3 H]HSO 4 : 1-(4-Sulfonic acid) butyl-3-methylimidazolium hydrogen sulfate
[EMIM]Cl: 1-Ethyl-3-methylimidazolium chloride
HPLC: Sắc ký lỏng hiệu năng cao
TLC: Sắc ký lớp mỏng
1 H-NMR: Phổ cộng hưởng từ hạt nhân proton.
IR: Phổ hồng ngoại.
HRMS: Phổ khối lượng độ phân giải cao.
XUNG ĐỘT LỢI ÍCH
Các tác giả tuyên bố rằng họ không có xung đột lợi ích.
ĐÓNG GÓP CỦA TÁC GIẢ
Phan Bích Hà đóng góp thực hiện thực nghiệm, thu thập số liệu, viết bản thảo. Trần Hoàng Phương đóng góp trong việc hỗ trợ khảo sát, góp ý và chỉnh sửa bản thảo.
LỜI CÁM ƠN
Nghiên cứu này được hỗ trợ kinh phí từ Đại học Quốc gia Thành phố Hồ Chí Minh, mã số 562-2020-18-01.
References
- Gong J; Katz MJ; Kerton FM. Catalytic conversion of glucose to 5-hydroxymethylfurfural using zirconium-containing metal-organic frameworks using microwave heating. RSC Advances 2018, 8 (55), 31618 - 31627. . ;:. Google Scholar
- Xia H; Xu S; Hu H; An J; Li C. Efficient conversion of 5-hydroxymethylfurfural to high-value chemicals by chemo- and bio-catalysis. RSC Advances 2018, 8 (54), 30875- 30886. . ;:. Google Scholar
- Putten RJ; van der Waal JC; de Jong E; Rasrendra CB; Heeres HJ; de Vries JG. Hydroxymethylfurfural, A versatile platform chemical made from renewable resources. Chemical Reviews 2013, 113 (3), 1499-1597. . ;:. PubMed Google Scholar
- Menegazzo F; Ghedini E; Signoretto M. 5-Hydroxymethylfurfural (HMF) production from real biomasses. Molecules 2018, 23 (9), 2201. . ;:. PubMed Google Scholar
- Guo W.. Continuous synthesis of 5-hydroxymethylfurfural from glucose using a combination of AlCl3 and HCl as catalyst in a biphasic slug flow capillary microreactor. Chemical Engineering Journal 2020, 381, 122754. . ;:. Google Scholar
- Chen J.. Conversion of fructose into 5-hydroxymethylfurfural catalyzed by recyclable sulfonic acid-functionalized metal-organic frameworks. Green Chemistry 2014, 16 (5), 2490-2499. . ;:. Google Scholar
- Rosatella A.A.. 5-Hydroxymethylfurfural (HMF) as a building block platform: Biological properties, synthesis and synthetic applications. Green Chemistry 2011, 13 (4), 754-793. . ;:. Google Scholar
- Yang Y.. Conversion of carbohydrates and lignocellulosic biomass into 5-hydroxymethylfurfural using AlCl3•6H2O catalyst in a biphasic solvent system. Green Chemistry 2012, 14 (2), 509-513. . ;:. Google Scholar
- Körner P.. The effect of different Brønsted acids on the hydrothermal conversion of fructose to HMF. Green Chemistry 2018, 20 (10), 2231-2241. . ;:. Google Scholar
- Mika L.T.. Catalytic conversion of carbohydrates to initial platform chemicals: Chemistry and Sustainability. Chemical Reviews 2018, 118 (2), 505- 613. . ;:. PubMed Google Scholar
- Tran P.H.. A highly selective and efficient method for the production of 5-hydroxymethylfurfural from dehydration of fructose using SACS/DES catalytic system. Fuel 2019, 246, 18-23. . ;:. Google Scholar
- Körner S.. Catalytic low-temperature dehydration of fructose to 5-hydroxymethylfurfural using acidic deep eutectic solvents and polyoxometalate catalysts. Frontiers in Chemistry 2019, 7 (661). . ;:. PubMed Google Scholar
- Zhang J.. Alcohol effect and the related mechanism on fructose dehydration into 5-hydroxymethylfurfural in the deep eutectic solvent of [Emim]Cl/Alcohol. ACS Sustainable Chemistry & Engineering 2016, 4 (7), 3995-4002. . ;:. Google Scholar
- Ullah Z.. Synthesis, characterization and the effect of temperature on different physicochemical properties of protic ionic liquids. RSC Advances 2015, 5(87), 71449-71461. . ;:. Google Scholar
- Nguyen L.H.T.. Synthesis of 5-hydroxymethylfurfural from monosaccharides catalyzed by superacid VNU-11-SO4 in 1-ethyl-3-methylimidazolium chloride ionic liquid. RSC Advances 2020, 10(65), 39687-39692. . ;:. Google Scholar
- Phan H.B.. A green and highly efficient synthesis of 5-hydroxymethylfurfural from monosaccharides using a novel binary ionic liquid mixture. Molecular Catalysis 2021, 503, 111428. . ;:. Google Scholar
- Ripin D.H.. pKa's of Inorganic and Oxo-Acids. The Evans. . 2005;:. Google Scholar
- D.J. Tao. SO3H-functionalized Brønsted acidic ionic liquids as efficient catalysts for the synthesis of isoamyl salicylate, RSC Advances 2014, 4 (1), 1-7. . ;:. Google Scholar

 Open Access
Open Access