Abstract
In this study, the magnetic Cu/CuFe2O4 nanocomposite was successfully prepared by a one-pot solvothermal method and evaluated for catalytic activity in the 4-nitrophenol (4-NP) reduction reaction and methylene blue (MB) degradation reaction. The structure, surface morphology, and properties of this catalyst were characterized by using several physicochemical methods such as Powder X-ray diffraction (PXRD), Fourier-transform infrared spectroscopy (FT-IR), UV-Vis diffuse reflectance spectroscopy (DRS), Brunauer–Emmett–Teller (BET), field emission scanning electron microscopy (FE-SEM), EDX mapping, and vibrating sample magnetometer (VSM). The Cu/CuFe2O4 catalyst is spherical in shape with an average diameter of about 145 nm and a BET surface area (SBET) of 52 m2.g-1. In both the 4-NP reduction and MB degradation reactions, this nanocomposite material showed high catalytic activity. The yield of 4-NP reduction reaction in the presence of NaBH4 was 82% after 5 minutes. In this reaction, Cu metal both plays the role of direct electron transfer from BH4- ions to 4-NP and participates in and promotes the electron transfer process between Cu+-Cu2+ and Fe2+-Fe3+ ion pairs in CuFe2O4. For MB degradation reaction, under the stimulation of UVA radiation with the presence of oxalic acid (H2C2O4) as a free radical-generating agent, the reaction yield was 98% after 40 minutes. In this process, Cu is an electron donor to reduce Fe3+ to Fe2+ in the CuFe2O4 structure, contributing to promoting the formation of highly active free radicals to decompose MB. The catalytic efficiency, crystal structure, and morphology of Cu/CuFe2O4 nanocomposite were stable over five consecutive uses in both two reactions.
MỞ ĐẦU
Thế kỷ 21 đánh dấu sự phát triển của nhiều ngành công nghiệp trên phạm vi toàn cầu. Một số ngành phát triển với tốc độ khá nhanh có thể kể đến như dược phẩm, thực phẩm, dệt nhuộm, sản xuất pin, sản xuất giấy, và công nghiệp nhựa… Tuy nhiên, cùng với sự phát triển thì những ngành công nghiệp trên cũng gây ra hệ lụy lớn đó chính là lượng nước thải được thải ra môi trường. Nguồn nước thải này bao gồm các chất độc vô cơ và hữu cơ, gây ảnh hưởng nghiêm trọng đến nguồn nước ngầm, môi trường tự nhiên, đời sống thủy sinh cũng như sức khỏe của con người. Riêng đối với chất độc hữu cơ thì thuốc nhuộm, hay phẩm màu hữu cơ là một trong những tác nhân chiếm hàm lượng chủ yếu 1 , 2 . Thuốc nhuộm hữu cơ là các hợp chất có cấu tạo gồm các vòng benzen cùng các nhóm phức chất mang màu khá bền và không bị phân hủy ở điều kiện thông thường. Đây là loại hóa chất được sử dụng rộng rãi trong các ngành công nghiệp như dệt may, da, giấy, dược phẩm, mỹ phẩm... Sau quá trình sản xuất, chúng được thải ra môi trường và nếu không được xử lý bằng quy trình phù hợp thì thuốc nhuộm sẽ trộn lẫn với mạch nước trên bề mặt, tiếp đến là mạch nước ngầm của trái đất gây độc hại, tác động tiêu cực đến môi trường sống của con người và hệ sinh thái 3 . Một ví dụ cụ thể có thể kể đến là methylene lue (MB). Khi nồng độ MB trong nước quá cao sẽ gây cản trở sự hấp thụ oxi từ không khí vào nước. Điều này làm ảnh hưởng quá trình sinh trưởng của các động thực vật, gây ra hiện tượng xáo trộn hoạt động của vi sinh vật và ảnh hưởng đến quá trình tự làm sạch của nước. Khi phơi nhiễm với MB, con người có thể bị các bệnh về mắt, da, đường hô hấp, đường tiêu hóa và thậm chí gây ra ung thư.
Ngoài ra, một trong những hợp chất quan trọng đóng vai trò trung gian trong tổng hợp hữu cơ, là nguồn nguyên liệu chính trong sản xuất dược phẩm, thuốc trừ sâu và phẩm nhuộm đó chính là các dẫn xuất nitro của phenol 4 , 5 , 6 . Các dẫn xuất này bao gồm ba loại đồng phân là o -nitrophenol, m -nitrophenol và p -nitrophenol hay còn được gọi là 4-nitrophenol (4-NP). Trong số các đồng phân này, 4-NP có độc tính cao cùng cấu trúc bền vững nhất. Đây là một trong những chất gây ô nhiễm chính trong nước thải công nghiệp và nông nghiệp 7 , gây nguy hiểm đến cả môi trường sinh thái và sức khỏe con người.
Chính vì lý do đó, việc xử lý loại bỏ MB cùng 4-NP ra khỏi nguồn nước sinh hoạt đang trở nên vô cùng cấp thiết đối với đời sống con người. Cho đến nay, một số phương pháp bao gồm cả vật lý, hóa học và sinh học đã được nghiên cứu nhằm loại bỏ các hợp chất nguy hiểm này 8 . Đối với 4-NP, hướng nghiên cứu đang thu hút được nhiều sự quan tâm đó là thực hiện phản ứng khử 4-NP độc hại để tạo thành 4-aminophenol (4-AP) thân thiện với môi trường 9 , 10 . Quá trình chuyển hóa 4-NP thành 4-AP có thể sử dụng phản ứng khử kim loại/bazơ 11 , sử dụng xúc tác đồng thể 12 , xúc tác hydro hóa dị thể 13 và phản ứng khử quang hóa 13 , 14 . Tuy nhiên, hiệu quả của các phương pháp này còn khá thấp, quá trình thu hồi chất xúc tác và loại bỏ bùn oxide kim loại sinh ra trong phản ứng còn khó khăn và tiêu tốn thời gian. Ngoài ra, những phản ứng này có sử dụng các tác chất độc hại, có thể gây ung thư và đột biến 15 . Những kết quả nghiên cứu gần đây nhất cho thấy, phản ứng khử 4-NP trong dung dịch nước khi sử dụng lượng dư natri borohydride (NaBH 4 ) và các chất xúc tác ferrite được xem là tối ưu do phản ứng đơn giản cùng hiệu quả khử 4-NP cao 16 , 17 , 18 , 19 . Riêng đối với MB, đã có rất nhiều phương pháp được đề nghị để xử lý loại phẩm nhuộm hữu cơ này trong nước thải 20 , 21 , 22 , 23 , 24 . Trong số đó, phương pháp đang được sử dụng khá phổ biến là phân hủy MB thông qua các quá trình oxi hóa nâng cao dựa trên các phản ứng có sử dụng xúc tác Fenton, cả Fenton đồng thể và dị thể 25 , 26 , 27 . So với Fenton dị thể thì nhược điểm lớn của Fenton đồng thể là khó xử lý lượng bùn sắt được sinh ra sau quá trình phản ứng. Chính vì vậy, trong phương pháp này xúc tác Fenton dị thể được sử dụng phổ biến hơn. Có thể kể đến một số loại xúc tác Fenton dị thể điển hình như oxide sắt 28 , goethite (a-FeOOH) 29 , Fe được cố định trên giá mang đất sét 30 hoặc zeolites 31 và đồng ferrite (CuFe 2 O 4 ) 32 . CuFe 2 O 4 là loại vật liệu ferrite có tính chất cơ lý tốt, độ dẫn điện cao, bền nhiệt và dễ dàng thu hồi khỏi dung dịch bằng từ trường ngoài nhờ có từ tính tốt 33 . Tuy nhiên, khi sử dụng làm xúc tác Fenton dị thể thì CuFe 2 O 4 có hiệu suất xúc tác không cao do vận tốc truyền tải electron thấp 34 , 35 . Những công bố gần đây cho thấy các hạt nano kim loại Cu cũng thực hiện được quá trình Fenton trong việc loại bỏ các chất ô nhiễm hữu cơ trong nước thải 36 , 37 , 38 , 39 . Vì vậy, việc kết hợp giữa Cu và CuFe 2 O 4 được xem là cách khả thi để tăng cường hiệu suất xúc tác của CuFe 2 O 4 . Ngoài ra, khi sử dụng làm xúc tác trong phản ứng khử 4-NP, một số công bố đã cho thấy CuFe 2 O 4 có hiệu suất xúc tác cao so với các loại vật liệu ferrite khác nhờ vào sự di chuyển hiệu quả của electron giữa các cặp ion Cu + -Cu 2+ và Fe 2+ -Fe 3+ tại vị trí bát diện 40 , 41 , 42 . Đồng thời, hoạt tính xúc tác của CuFe 2 O 4 còn được tăng cường khi chế tạo nanocomposite trên cơ sở kim loại quý/ CuFe 2 O 4 43 , 44 , 45 . Tuy nhiên, giá thành cao cùng sự khan hiếm của kim loại quý đã gây trở ngại cho việc ứng dụng của loại vật liệu này trong thực tế. Với mục đích thay thế các kim loại quý này bằng một vật liệu dễ kiếm, giá thành rẻ và thân thiện với môi trường thì các hạt nano Cu kim loại là một lựa chọn đầy triển vọng. Gần đây nhất, Li và các cộng sự đã tổng hợp nanocomposite Cu/CuFe 2 O 4 bằng phương pháp nhiệt dung môi để làm xúc tác Fenton trong phản ứng phân hủy MB 46 . Kết quả đã chứng minh nhờ hiệu ứng đồng vận giữa Cu và CuFe 2 O 4 đã thúc đẩy quá trình phân hủy của MB. Nhóm của Koley cùng các cộng sự cũng sử dụng composite Cu/CuFe 2 O 4 @C làm xúc tác cho phản ứng tổng hợp 2-methylfuran từ furfural có nguồn gốc từ sinh khối 47 . Tuy nhiên cho đến nay vẫn còn khá ít các nghiên cứu sử dụng nanocomposite Cu/CuFe 2 O 4 làm xúc tác cho phản ứng khử 4-NP.
Trong nghiên cứu này, nanocomposite Cu/CuFe 2 O 4 từ tính được tổng hợp bằng phương pháp nhiệt dung môi đơn giản một giai đoạn. Vật liệu được sử dụng làm xúc tác trong cả hai phản ứng, bao gồm phản ứng khử 4-NP thành 4-AP khi có mặt NaBH 4 là chất cho electron và phản ứng phân hủy MB, với sự có mặt của oxalic acid (H 2 C 2 O 4 ) đóng vai trò tác nhân tạo gốc tự do. Vai trò của từng hợp phần Cu và CuFe 2 O 4 trong xúc tác Cu/CuFe 2 O 4 đã được đề cập đến trong hai cơ chế phản ứng đề nghị trong nghiên cứu này. Ngoài ra, khả năng thu hồi và tái sử dụng của vật liệu xúc tác cũng được khảo sát.
VẬT LIỆU VÀ PHƯƠNG PHÁP
Vật liệu
Hai tiền chất của đồng và sắt là copper (II) chloride dihydrate (CuCl 2 .2H 2 O) và iron (III) chloride hexahydrate (FeCl 3 .6H 2 O) có xuất xứ từ Trung Quốc với độ tinh khiết 99,0%, polyethylene glycol (PEG-6.000) 99,0%, ammonium acetate (NH 4 OAc) 98,0%, dung môi ethylene glycol (EG) 96,0% và phẩm nhuộm methylene blue (C 16 H 18 N 3 ClS) 99,6% đều là dạng thương mại của Trung Quốc. Polyvinylpyrrolidone (PVP-1.300.000), sodium borohydride (NaBH 4 ) và 4-nitrophenol (4-NP) đều có độ tinh khiết 99,0%, là hàng thương mại của Sigma-Aldrich. Tất cả các hóa chất được sử dụng trực tiếp mà không cần phải tinh chế lại.
Phương pháp nghiên cứu
Cấu trúc tinh thể và thành phần pha của vật liệu được xác định từ giản đồ nhiễu xạ tia X dạng bột (PXRD) với đối âm cực là đồng (Cu). Giản đồ PXRD được phân tích trên thiết bị D2 PHARSER (Bruker, Đức). Quá trình phân tích được thực hiện khi thay đổi góc 2θ từ 10° đến 80° với bước chuyển 0,02°/phút. Thành phần hóa học được phân tích bằng phổ hồng ngoại biến đổi Fourier (FT-IR), được đo trên máy quang phổ TENSOR 27 (Bruker, Đức) trong vùng số sóng từ 4000 cm -1 đến 400 cm -1 với độ phân giải là 4 cm -1 . Vật liệu dạng bột trước khi phân tích được nghiền mịn và sấy trong 24 giờ ở 80°C. Sau đó một lượng nhỏ mẫu (~2-3 mg) được ép viên với KBr theo tỷ lệ khối lượng mẫu và KBr là 1:100 ở lực nén 250 kN. Hình thái học vật liệu được phân tích bằng ảnh hiển vi điện tử quét (FE-SEM) trên thiết bị S–4800 với thế gia tốc 5 kV. Sự phân bố của các nguyên tố hiện diện trên bề mặt được xác định bằng ảnh EDX mapping, được phân tích từ hệ EMAX ENERGY kết hợp trên thiết bị S-4800. Các tính chất từ của vật liệu bao gồm độ từ hóa bão hòa (M s ), độ từ dư (M r ), lực kháng từ (H c ) và đường cong từ trễ được phân tích bằng phương pháp từ kế mẫu rung (VSM) trên thiết bị System ID: EV11, SN:2010062. Quá trình phân tích được đo với giá trị từ trường ngoài từ -12.000 đến +12.000 Oe. Diện tích bề mặt vật liệu được xác định từ đường cong hấp phụ - giải hấp phụ nitrogen, được phân tích trên máy NOVA 1000e analyzer (Quantachrome Instruments). Phổ phản xạ khuếch tán UV-Vis (DRS), đo trên máy quang phổ Perkin-Elmer Lambda 850, được sử dụng để tính giá trị năng lượng vùng cấm (E g ) của vật liệu. Phổ tử ngoại – khả kiến (UV-Vis) được đo bằng máy UV-Vis V-670_Jasco trong vùng bước sóng từ 200 - 800 nm, với tốc độ 400 nm/phút.
Tổng hợp Cu/CuFe2O4 bằng phương pháp nhiệt dung môi
Quy trình tổng hợp vật liệu nanocomposite Cu/CuFe 2 O 4 được tiến hành theo các bước như được mô tả trên Figure 1 . Đầu tiên, dung dịch tiền chất kim loại được điều chế bằng cách hòa tan 1,60 mmol CuCl 2 .2H 2 O và 3,20 mmol FeCl 3 .6H 2 O trong 20 mL ethylene glycol. Tiếp đến, 0,75 g polyethylene glycol (PEG-6.000) và 0,20 g polyvinylpyrrolidone (PVP-1.300.000) được lần lượt thêm vào và hỗn hợp được tiếp tục khuấy trong 0,5 giờ. Sau đó, NH 4 OAc (180 mmol) được thêm vào và hỗn hợp lại tiếp tục được khuấy cho đến khi thu được dung dịch màu xanh đồng nhất. Cuối cùng, dung dịch được chuyển vào bình thủy nhiệt bằng Teflon - thép không gỉ (dung tích 80 mL) và ủ nhiệt ở 200°C trong 11 giờ. Sau phản ứng, bình thủy nhiệt được làm lạnh đến nhiệt độ phòng, lọc và rửa sạch sản phẩm bằng nước và ethanol ba lần. Cuối cùng, sản phẩm được sấy đông khô trong 8 giờ, thu được vật liệu Cu/CuFe 2 O 4.
Figure 1 . Sơ đồ quy trình tổng hợp Cu/CuFe 2 O 4 bằng phương pháp nhiệt dung môi
Khảo sát hoạt tính xúc tác khử 4-NP
Hoạt tính xúc tác của vật liệu Cu/CuFe 2 O 4 được khảo sát thông qua phản ứng khử 4-NP thành 4-AP. Đầu tiên hỗn hợp gồm 10 mL nước khử ion và 250 µL dung dịch 4-NP (0,005 mol.L -1 ) được trộn với 10 mL dung dịch NaBH 4 (0,5 mol.L -1 ). Tiếp đến, 750 µL huyền phù của Cu/CuFe 2 O 4 (40 mg.mL -1 ) được cho vào dung dịch trên để xúc tác cho phản ứng xảy ra. Sự thay đổi nồng độ của 4-NP được xác định bằng phổ UV-Vis thông qua sự thay đổi cường độ hấp thu của đỉnh ở vị trí 400 nm theo thời gian và phương trình đường chuẩn của 4-NP. Khả năng khử 4-NP thành 4-AP được tính theo công thức (1):
Trong đó %R là khả năng khử, C t và C o (mol.L -1 ) lần lượt là nồng độ tại thời điểm t và nồng độ ban đầu của 4-NP, được xác định thông qua phương pháp dựng đường chuẩn.
Khảo sát hoạt tính xúc tác phân hủy MB
Hoạt tính Fenton quang xúc tác của vật liệu được đánh giá thông qua sự phân hủy MB với tác nhân tạo gốc tự do cho phản ứng là H 2 C 2 O 4 (10 - 3 mol.L - 1 ) dưới bức xạ UVA (320 < λ < 400 nm). Toàn bộ thời gian trong suốt quá trình khảo sát, phản ứng được thực hiện trong một buồng kín với nhiệt độ luôn được duy trì ở 29 – 31 o C. Đầu tiên, 0,050 g chất xúc tác được thêm vào 250 mL dung dịch có chứa MB (5×10 -5 mol.L -1 ) và H 2 C 2 O 4 (10 -3 mol.L -1 ). Hỗn hợp phản ứng có giá trị pH ở khoảng 7 và được khuấy liên tục bằng máy khuấy trục IKA RW 20 digital. Để đảm bảo quá trình hấp phụ MB lên bề mặt xúc tác đạt trạng thái cân bằng, hỗn hợp được khuấy đều trong bóng tối suốt 25 phút (thời gian cân bằng hấp phụ 25 phút được xác định thông qua các khảo sát sơ bộ trước đó, khi theo dõi nồng độ MB ban đầu gần như không thay đổi trong hệ xúc tác dưới điều kiện không chiếu sáng). Sau đó, hệ phản ứng được chiếu xạ dưới nguồn sáng UVA (9 W Radium 78) được đặt cách bề mặt hỗn hợp phản ứng 17 cm. Sau mỗi 5 phút, 10 mL dung dịch được rút ra khỏi hệ, xúc tác được tách ra khỏi dung dịch này bằng nam châm đất hiếm. Nồng độ MB còn lại trong dung dịch được xác định bằng phương pháp phổ hấp thu UV-Vis ở bước sóng 664 nm trên thiết bị Helios Omega UV-VIS (Thermo Fisher Scientific, USA). Từ giá trị độ hấp thu và dựa vào đường chuẩn của MB để xác định nồng độ MB còn lại trong dung dịch. Khả năng phân hủy MB được tính theo công thức (2):
Trong đó %H là khả năng phân hủy, C t và C o (mol.L -1 ) lần lượt là nồng độ tại thời điểm t và nồng độ ban đầu của MB, được xác định thông qua phương pháp dựng đường chuẩn.
Khảo sát khả năng thu hồi và tái sử dụng của vật liệu
Khả năng thu hồi và tái sử dụng của vật liệu Cu/CuFe 2 O 4 được đánh giá trong cả hai phản ứng khử 4-NP và phân hủy MB. Vật liệu sau quá trình khảo sát được thu hồi bằng nam châm đất hiếm, được rửa lại bằng cách khuấy trong nước và ethanol. Sau đó, xúc tác được cô lập, sấy khô trong 12 giờ ở 90 o C và tiếp đến là thực hiện lại cả hai phản ứng trong điều kiện tương tự như ban đầu.
KẾT QUẢ VÀ THẢO LUẬN
Giản đồ PXRD
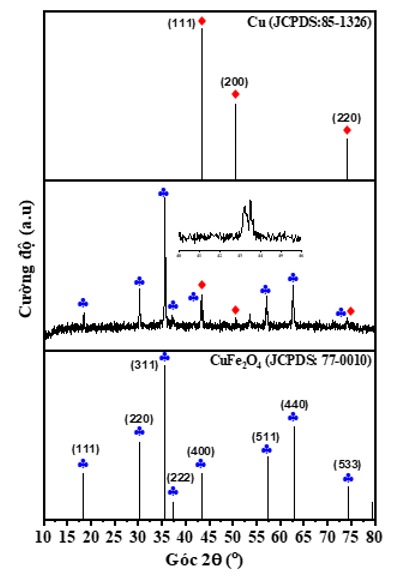
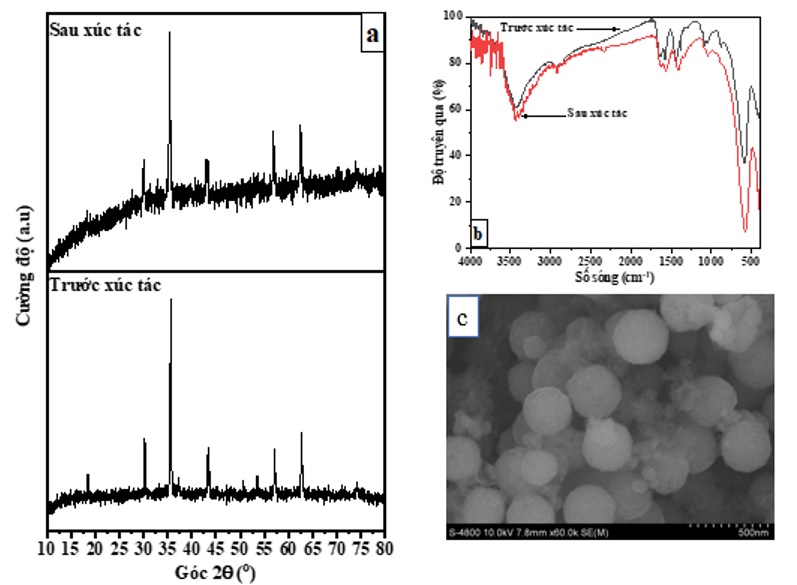
Giản đồ PXRD của nanocomposite Cu/CuFe 2 O 4 được trình bày trên Figure 2 . Cấu trúc spinel lập phương của CuFe 2 O 4 (JCPDS: 77-0010) được đặc trưng bởi các đỉnh nhiễu xạ ở 2θ = 18,5°; 30,2°; 35,6 o ; 37,3 o ; 57,1° và 62,8° lần lượt tương ứng với các mặt mạng (111), (220), (311), (222), (511) và (440) 48 , 17 . Kết quả PXRD cũng quan sát thấy các đỉnh nhiễu xạ (được ký hiệu ♦) đặc trưng cho tinh thể Cu (JCPDS: 85-1326). Đỉnh nhiễu xạ đặc trưng cho mặt mạng (220) của Cu và (533) của CuFe 2 O 4 bị chồng chập tại 2θ = 74,5 o . Giản đồ PXRD của Cu/CuFe 2 O 4 cho một đỉnh nhiễu xạ có dạng đỉnh đôi tại 2θ khoảng 43,0 o . Nguyên nhân của hiện tượng này có thể là do đây là vị trí xuất hiện đồng thời đỉnh nhiễu xạ đặc trưng cho cả mặt mạng (111) của Cu và (400) của CuFe 2 O 4 17 . Sự hiện diện của tinh thể Cu trong thành phần của nanocomposite Cu/CuFe 2 O 4 còn được xác nhận bằng tín hiệu đỉnh nhiễu xạ tại 2θ = 50,8 o , tương ứng với mặt phẳng tinh thể (200) trong cấu trúc lập phương của Cu. Sự tồn tại của Cu kim loại là do trong quá trình nhiệt dung môi này, dung môi sử dụng là ethylene glycol. Đây là loại dung môi có tính khử mạnh, nên ở 200 o C một số ion Cu 2+ bị khử xuống Cu 48 . Kim loại Cu không những có tính chất hóa lý tốt cùng độ dẫn điện cao mà còn có hoạt tính xúc tác cao trong việc khử 4-NP với chất khử NaBH 4 . Gần đây một số nghiên cứu cho thấy hạt nano Cu xúc tác rất hiệu quả cho quá trình khử 4-NP thành 4-AP 49 , 50 , 51 , 52 .
Phổ FT-IR
Figure 3 là phổ FT-IR của nanocomposite Cu/CuFe 2 O 4 . Mũi hấp thu tại 3440 cm -1 và 1640 cm -1 là dao động kéo dãn và dao động biến dạng liên kết O-H của H 2 O được hấp phụ trên bề mặt của Cu/CuFe 2 O 4 . Mũi hấp thu yếu tại 2910 cm -1 và mũi tại 1440 cm -1 là dao động kéo dãn và dao động biến dạng của nhóm -CH 2 do dư lượng PEG còn lại trong vật liệu. Tín hiệu PEG còn quan sát thấy trên phổ FT-IR tại các số sóng 1572, 1104 và 1041 cm -1 . Mũi tại số sóng 1375 cm -1 là dao động kéo dãn của nhóm CO 3 2- . Nguyên nhân có sự xuất hiện của mũi hấp thu trên là do các oxide sắt (III) hoặc sắt (III) hydroxide dễ bị carbon hóa bởi CO 2 trong khí quyển 53 . Sự hình thành của liên kết Fe-O và Cu-O trong CuFe 2 O 4 được xác định thông qua hai mũi hấp thu tại 590 cm -1 , đặc trưng cho liên kết Fe-O trong cấu trúc tứ diện và 430 cm -1 , đặc trưng cho liên kết Cu-O trong cấu trúc bát diện 54 , 19 . Mũi hấp thu yếu tại 890 cm -1 là dao động biến dạng trong mặt phẳng của liên kết Fe-O 55 .
Ảnh FE-SEM và ảnh EDX mapping
Figure 4 . Ảnh FE-SEM (a, b), biểu đồ phân bố kích thước (c) và ảnh EDX mapping của nanocomposite Cu/CuFe 2 O 4
Hình thái học và sự phân bố các nguyên tử trong nanocomposite Cu/CuFe 2 O 4 được phân tích bằng ảnh FE-SEM và ảnh EDX mapping. Kết quả FE-SEM ( Figure 4 a, b) cho thấy Cu/CuFe 2 O 4 có dạng hình cầu với bề mặt hạt tương đối nhẵn và ít ghồ ghề. Các hạt ở trạng thái đa phân tán với kích thước không đồng đều. Nguyên nhân là do sự hình thành và tái sắp xếp của hai thành phần là Cu và CuFe 2 O 4 trong vật liệu. Đầu tiên, hỗn hợp hai muối gồm CuCl 2 và FeCl 3 được hòa tan trong dung môi ethylene glycol. Tiếp đến, các chất bảo vệ bề mặt là PEG và PVP cùng NH 4 OAc được thêm vào dung dịch ethylene glycol đã có chứa các cation hòa tan là Cu 2+ và Fe 3+ . Quá trình dung nhiệt xảy ra, NH 4 OAc sẽ bị phân hủy và hình thành các bong bóng khí NH 3 . Ở nhiệt độ cao, các cation Cu 2+ và Fe 3+ sẽ hình thành các mầm kết tinh và phát triển thành các tinh thể CuFe 2 O 4 . Một số hạt CuFe 2 O 4 sẽ kết tụ lại và gắn kết trên bề mặt các bóng khí NH 3 . Ngoài ra, trong hỗn hợp phản ứng còn có sự tạo thành của Cu kim loại, do cation Cu 2+ bị khử bởi dung môi ethylene glycol ở nhiệt độ cao. Chính sự hình thành, phát triển và gắn kết của hai thành phần Cu và CuFe 2 O 4 xảy ra đồng thời đã làm cho kích thước của nanocomposite Cu/CuFe 2 O 4 không đồng đều.
Biểu đồ phân bố kích thước hạt ( Figure 4 c) thu được sau khi xử lý ảnh FE-SEM bằng phần mềm ImageJ cho thấy vật liệu có đường kính phân bố trong khoảng 50- 250 nm, với đường kính trung bình ~145 nm. Qua phân tích EDX mapping thì vật liệu chỉ bao gồm các nguyên tố là Cu, Fe và O; không có sự hiện diện của nguyên tố lạ. Đồng thời các nguyên tố Cu, Fe và O phân bố đồng đều trong toàn bộ khối cấu trúc vật liệu. Như vậy, từ các kết quả trên cho thấy qua quá trình nhiệt dung môi một giai đoạn đã tổng hợp thành công nanocomposite Cu/CuFe 2 O 4 có dạng hạt cầu với đường kính trung bình ~145 nm.
Xác định diện tích bề mặt bằng phép đo đường cong hấp phụ - giải hấp phụ nitrogen
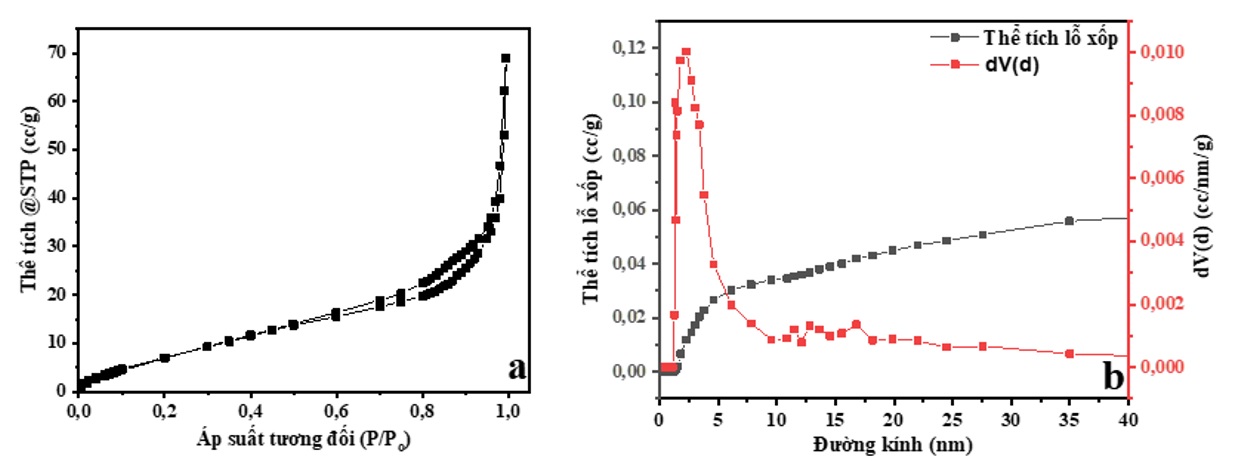
Diện tích bề mặt của Cu/CuFe 2 O 4 được xác định từ đường cong đẳng nhiệt hấp phụ - giải hấp phụ nitrogen bằng phương pháp phân tích BET (Brunauer-Emmett-Teller) đa điểm. Sự phân bố kích thước lỗ xốp trong vật liệu được tính toán dựa trên phương pháp BJH (Barrett-Joyner-Halenda). Đường cong hấp phụ - giải hấp phụ nitrogen của Cu/CuFe 2 O 4 ( Figure 5 a) thuộc loại IV, dạng H, đặc trưng của vật liệu mao quản trung bình. Tại vùng áp suất thấp là quá trình hấp phụ trên bề mặt vật liệu, tiếp đến hàm lượng khí hấp phụ tăng khi áp suất tăng. Điều này gây ra bởi sự ngưng tụ mao quản, và từ đó xuất hiện vòng trễ. Diện tích bề mặt BET của Cu/CuFe 2 O 4 (S BET ) được xác định là 52 m 2 .g -1 . Kích thước và sự phân bố lỗ xốp trong vật liệu ( Figure 5 b) được tính toán bằng phương pháp BJH cho kết quả giá trị lớn nhất của đường kính lỗ xốp là khoảng 2 nm, với thể tích lỗ xốp là 0,117 cc.g -1 .
Figure 5 . Đường cong hấp phụ-giải hấp phụ nitrogen và giản đồ phân bố kích thước lỗ xốp của Cu/CuFe 2 O 4
Tính chất quang và từ tính của vật liệu
Tính chất quang của vật liệu được phân tích bằng phổ DRS trong vùng bước sóng từ 250 đến 800 nm. Kết quả DRS ( Figure 6 ) của Cu/CuFe 2 O 4 cho thấy vật liệu có thể hấp thu ánh sáng tốt cả trong vùng tử ngoại và vùng ánh sáng khả kiến. Năng lượng vùng cấm (E g ) được xác định bằng cách áp dụng công thức Tauc (3):
Trong đó, α là hệ số hấp thu, A là hằng số, h (eV×giây) là hằng số Planck, υ (giây -1 ) là tần số photon và E g (eV) là năng lượng vùng cấm. Giá trị n = 1/2 cho vật liệu bán dẫn có vùng cấm trực tiếp. Giá trị E g được xác định từ phép ngoại suy tuyến tính của đồ thị (αhυ) 2 theo năng lượng E (E = hυ = 1240/λ), với λ (nm) là bước sóng 56 . Giá trị E g của vật liệu Cu/CuFe 2 O 4 được xác định là 1,22 eV.
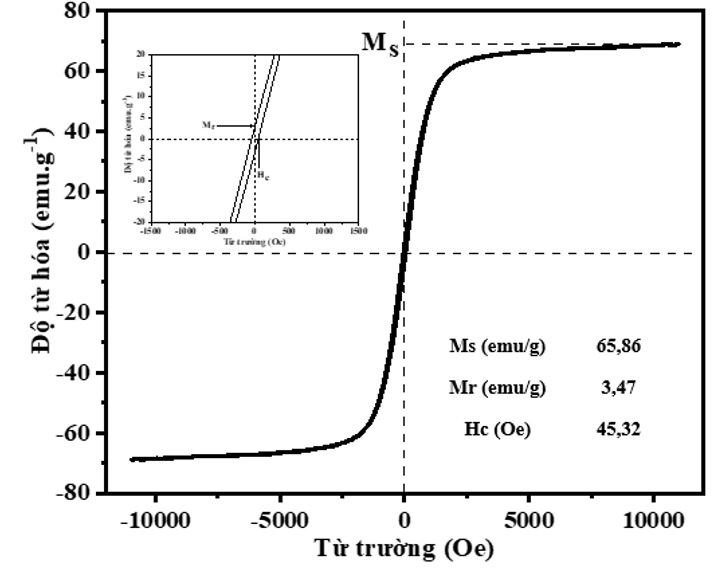
Kết quả đo từ tính của Cu/CuFe 2 O 4 bằng phương pháp VSM được thể hiện qua đường cong từ trễ cùng các giá trị độ từ hóa bão hòa (M s ), độ từ dư (M r ) và lực kháng từ (H c ) được cho trong bảng trên Figure 7 . Kết quả đường cong VSM cho thấy Cu/CuFe 2 O 4 có độ kháng từ thấp với độ trễ không rõ ràng, giá trị M s của CuFe 2 O 4 là 68,86 emu.g -1 . Như vậy, kết quả này đã xác minh được sự tổng hợp thành công nanocomposite Cu/CuFe 2 O 4 có tính chất thuận từ 48 . Điều này sẽ giúp cho vật liệu được cô lập dễ dàng khỏi dung dịch bằng từ trường ngoài sau quá trình phản ứng.
Hoạt tính xúc tác của Cu/CuFe2O4
Hoạt tính xúc tác của vật liệu Cu/CuFe 2 O 4 được khảo sát trong phản ứng khử 4-NP khi có mặt lượng dư NaBH 4 và phản ứng phân hủy MB với tác nhân tạo gốc tự do là H 2 C 2 O 4 . Trong phản ứng khử 4-NP, quá trình phản ứng được đánh giá qua sự thay đổi cường độ của đỉnh hấp thu ở vị trí 400 nm trên phổ UV-Vis của 4-NP theo thời gian. Kết quả phổ UV-Vis trên Figure 8 a cho thấy sau khi thêm NaBH 4 , đỉnh hấp thu đặc trưng của 4-NP ở bước sóng 317 nm đã dịch chuyển về bước sóng 400 nm. Điều này là do sự hình thành của ion 4-nitrophenolate từ 4-NP khi có mặt NaBH 4 , kèm theo là hiện tượng dung dịch chuyển từ màu vàng nhạt sang màu vàng sáng 17 . Tiếp đến xúc tác Cu/CuFe 2 O 4 được thêm vào. Khi có mặt chất xúc tác thì mũi hấp thu ở bước sóng 400 nm, đặc trưng của 4-nitrophenolate, giảm theo thời gian. Trong khi đó, cường độ mũi hấp thu ở bước sóng 317 nm, là mũi hấp thu của 4-AP, lại tăng theo thời gian ( Figure 8 b). Sau thời gian phản ứng là 5 phút, theo công thức (1), hiệu suất khử 4-NP thành 4-AP khi sử dụng xúc tác Cu/CuFe 2 O 4 đạt được là khoảng 82% ( Figure 8 c). Quá trình khử 4-NP thành 4-AP xảy ra theo cơ chế xúc tác dị thể trên bề mặt nanocomposite Cu/CuFe 2 O 4 như được mô tả trên Figure 9 . Trong phản ứng này ion BH 4 - , được tạo ra sau quá trình ion hóa NaBH 4 , đóng vai trò vừa là chất cho điện tử cũng vừa là nguồn cung cấp hydrogen đang sinh 17 . Khi xúc tác Cu/CuFe 2 O 4 được thêm vào phản ứng, thì trước tiên BH 4 - và 4-NP sẽ khuếch tán từ dung dịch đến hấp phụ trên bề mặt Cu/CuFe 2 O 4 . Vật liệu Cu/CuFe 2 O 4 đóng vai trò làm chất trung gian để chuyển electron từ chất cho là BH 4 - sang chất nhận là 4-NP. Về mặt nhiệt động học, phản ứng tự xúc tác giữa 4-NP và NaBH 4 là có thể xảy ra. Tuy nhiên, phản ứng này bị khống chế lớn về mặt động học do sự khác nhau về thế oxi hóa khử giữa cặp borate/borohydride và cặp 4-NP/4-AP 57 , 58 , 59 . Chính vì vậy, việc sử dụng xúc tác Cu/CuFe 2 O 4 làm chất trung gian để chuyển electron sẽ giúp cho phản ứng vượt được rào cản động học và tạo thành 4-AP 60 . Ngoài ra, Cu 2+ rất dễ chuyển về Cu + khi có mặt NaBH 4 và Cu cũng đóng vai trò là chất cho electron để khử Fe 3+ thành Fe 2+ trong cấu trúc CuFe 2 O 4 , để từ đó Fe 2+ tham gia vào phản ứng khử 4-NP. Chính sự thay đổi trạng thái oxi hóa khử giữa các cặp ion Cu + -Cu 2+ và Fe 2+ -Fe 3+ này đã góp phần tăng cường hoạt tính xúc tác của nanocomposite Cu/CuFe 2 O 4 40 , 41 , 42 . Như vậy, trong cơ chế này hạt nano kim loại Cu đóng hai vai trò trong quá trình xúc tác của nanocomposite Cu/CuFe 2 O 4 . Vai trò thứ nhất là chuyển electron trực tiếp từ ion BH 4 - sang 4-NP và vai trò thứ hai là hạt nano Cu kim loại tham gia và thúc đẩy quá trình chuyển electron giữa các cặp ion Cu + -Cu 2+ và Fe 2+ -Fe 3+ trong CuFe 2 O 4 17 .
Figure 8 . Phổ UV–Vis của (a) dung dịch 4-NP ban đầu và sau khi thêm NaBH 4 , (b) trong quá trình phản ứng với chất xúc tác là Cu/CuFe 2 O 4 và (c) hàm lượng 4-NP phân hủy theo thời gian trong quá trình phản ứng
Figure 9 . Cơ chế đề nghị cho phản ứng khử 4-NP thành 4-AP với xúc tác Cu/CuFe 2 O 4 khi có mặt NaBH 4
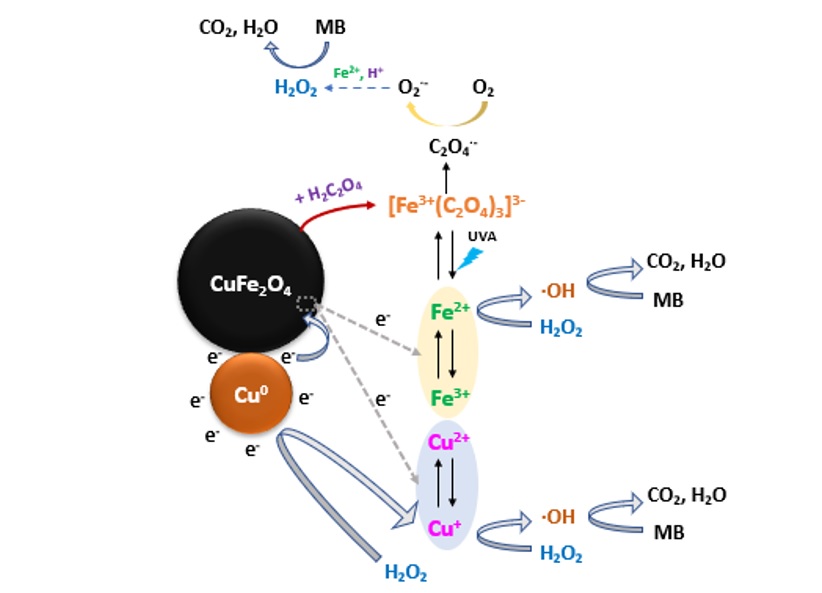
Kết quả khảo sát hoạt tính xúc tác của Cu/CuFe 2 O 4 trong phản ứng phân hủy MB ở các điều kiện khác nhau được thể hiện trong Figure 10 . Thông qua sự thay đổi nồng độ của MB, có thể thấy quá trình Fenton quang xúc tác chỉ xảy ra khi có mặt đầy đủ các yếu tố gồm Cu/CuFe 2 O 4 , dung dịch OA cùng sự kích thích của bức xạ UVA. Sau thời gian chiếu xạ 40 phút, hiệu suất phân hủy MB, tính theo công thức (2), khi sử dụng xúc tác Cu/CuFe 2 O 4 đạt được là 98%. Quá trình xúc tác Cu/CuFe 2 O 4 tham gia vào phản ứng phân hủy MB được mô tả trên Figure 11 . Khi có mặt H 2 C 2 O 4 , tâm Fe hoạt tính trên bề mặt của tinh thể CuFe 2 O 4 đã tương tác với H 2 C 2 O 4 để tạo ra phức chất trung gian [≡Fe(C 2 O 4 ) 3 ] 3- . Dưới sự kích thích của bức xạ UVA, các phức chất sẽ bị kích thích và sản sinh ra gốc tự do ● OH, O 2 ●- và hợp chất trung gian là H 2 O 2 (phương trình 1-5 61 , 62 ). Hợp chất trung gian H 2 O 2 sau đó sẽ phản ứng với Cu kim loại (phương trình 6-10 39 , 63 ) để tiếp tục tạo thành các tiểu phân có chứa oxy hoạt tính cao là ● OH, O 2 ●- và HO 2 ● .
[≡Fe(C 2 O 4 ) 3 ] 3- + hʋ → Fe 2+ +2C 2 O 4 2- + C 2 O 4 ●- (1)
C 2 O 4 ●- + O 2 → O 2 ●- + 2CO 2 (2)
O 2 ●- + H + → HO 2 ● (3)
HO 2 ● + HO 2 ● → H 2 O 2 + O 2 (4)
Fe 2+ + H 2 O 2 + 3C 2 O 4 2- → [≡Fe(C 2 O 4 ) 3 ] 3- + OH - + ● OH (5)
Cu + H 2 O 2 → Cu 2+ + 2OH - (6)
2Cu + H 2 O 2 + 2H + → 2Cu + + 2H 2 O (7)
Cu 2+ + H 2 O 2 → Cu + + HO 2 ● + H + (8)
Cu + + H 2 O 2 → Cu 2+ + HO ● + HO - (9)
Cu + + O 2 → Cu 2+ + O 2 ●- (10)
Figure 11 . Cơ chế đề nghị cho phản ứng phân hủy MB với xúc tác Cu/CuFe 2 O 4 khi có sự hiện diện của H 2 C 2 O 4
Ngoài ra, Cu cũng đóng vai trò là chất cho electron để khử Fe 3+ thành Fe 2+ trong cấu trúc CuFe 2 O 4 và Fe 2+ lại tiếp tục xúc tiến sự tạo thành của gốc tự do ● OH (phương trình 11, 12). Cũng vào thời điểm này, Cu 2+ trong CuFe 2 O 4 cũng bị khử thành Cu + (phương trình 13), sau đó Cu + lại phản ứng với H 2 O 2 và lại tiếp tục tạo ra gốc tự do ● OH (phương trình 9). Ngoài ra, về mặt nhiệt động học, Cu + vẫn có khả năng khử Fe 3+ xuống Fe 2+ (phương trình 14), và sản phẩm của quá trình này tiếp đến lại hình thành thêm gốc ● OH và HO 2 ● 64 . Như vậy, trong hệ phản ứng Cu/CuFe 2 O 4 - H 2 C 2 O 4 , tất cả các tiểu phân có chứa oxy hoạt tính sinh ra, bao gồm cả ● OH, O 2 ●- và HO 2 ● , sẽ tấn công MB, hình thành các hợp chất trung gian, và cuối cùng là quá trình khoáng hóa tạo ra CO 2 và H 2 O (phương trình 15).
Cu + 2Fe 3+ → 2Fe 2+ + 2Cu 2+ (11)
Fe 2+ + H 2 O 2 → Fe 3+ + HO ● + OH - (12)
2Cu 2+ + H 2 O 2 → Cu + + HO 2 - (13)
Cu + + Fe 3+ → Fe 2+ + Cu 2+ (14)
HO ● /O 2 ●- /HO 2 ● + MB → Hợp chất trung gian → CO 2 + H 2 O (15)
Khả năng thu hồi và tái sử dụng
Figure 12 . Hoạt tính xúc tác của nanocomposite Cu/CuFe2O4 ở năm lần sử dụng liên tiếp nhau trong phản ứng khử 4-NP (a) và phản ứng phân hủy MB (b)
Khả năng tái sử dụng của vật liệu được đánh giá thông qua khảo sát hoạt tính xúc tác của Cu/CuFe 2 O 4 ở năm lần sử dụng liên tiếp nhau. Trong cả hai phản ứng khử 4-NP và phân hủy MB, vật liệu sau quá trình khảo sát đầu tiên đã được thu hồi bằng nam châm đất hiếm và rửa lại với nước và ethanol. Tiếp đến, xúc tác rắn được cô lập, sấy khô trong 12 giờ ở 90 o C và thực hiện lại quá trình phản ứng trong điều kiện tương tự như ban đầu. Hoạt tính xúc tác của vật liệu trong cả hai phản ứng sau năm lần sử dụng được thể hiện trên Figure 12 . Kết quả cho thấy sau năm lần sử dụng liên tiếp, hiệu quả xúc tác của nanocomposite Cu/CuFe 2 O 4 trong cả hai phản ứng vẫn được duy trì, không thay đổi. Độ ổn định về mặt thành phần, cấu trúc tinh thể và hình thái học của xúc tác Cu/CuFe 2 O 4 sau khi thực hiện năm phản ứng liên tiếp nhau cũng gần như không có sự thay đổi. Điều này được thể hiện thông qua kết quả của giản đồ PXRD, phổ FT-IR và ảnh FESEM của vật liệu trước và sau khi xúc tác như được trình bày tại Figure 13 .
Figure 13 . Giản đồ PXRD (a), phổ FT-IR (b) của Cu/CuFe 2 O 4 trước và sau khi xúc tác cho hai phản ứng khử 4-NP, phân hủy MB và ảnh FE-SEM sau năm lần phản ứng liên tiếp (c).
Kết quả PXRD cho thấy Cu/CuFe 2 O 4 sau quá trình xúc tác vẫn giữ được cấu trúc đặc trưng cho cấu trúc spinel ferrite của CuFe 2 O 4 . Các đỉnh nhiễu xạ của Cu kim loại vẫn còn quan sát được trên giản đồ. Tuy nhiên, cường độ của các đỉnh này khá yếu và đường nền của giản đồ PXRD bị nhiễu khá nhiều so với giản đồ PXRD của vật liệu trước khi xúc tác. Nguyên nhân có thể là do sau các chu kỳ xúc tác liên tiếp nhau, sự trao đổi electron và sự thay đổi trạng thái oxi hóa – khử của các tiểu phân trong tinh thể xảy ra liên tục đã làm cho tinh thể kém ổn định và sự sắp xếp các tiểu phân không còn chặt chẽ so với ban đầu. Thành phần của vật liệu sau xúc tác gần như không có sự thay đổi. Phổ FT-IR của Cu/CuFe 2 O 4 sau xúc tác vẫn giữ nguyên các mũi hấp thu mạnh tại 590 cm -1 (Fe tu dien -O) và 430 cm -1 (Cu bat dien -O) 19 , 54 . Kết quả ảnh FE-SEM cho thấy sau năm lần phản ứng liên tiếp, nanocomposite Cu/CuFe 2 O 4 vẫn giữ được hình thái hạt cầu. Như vậy, các kết quả trên đã chứng tỏ rằng vật liệu Cu/CuFe 2 O 4 có khả năng thu hồi và tái sử dụng tốt. Ngoài ra, xúc tác được chế tạo bằng phương pháp nhiệt dung môi có độ ổn định cao trong điều kiện phản ứng. Điều này hứa hẹn sẽ mang lại hiệu quả về mặt kinh tế khi đưa vật liệu ứng dụng vào thực tế.
KẾT LUẬN
Vật liệu nanocomposite Cu/CuFe 2 O 4 có từ tính đã được điều chế thành công bằng quá trình nhiệt dung môi một giai đoạn nhằm làm xúc tác cho hai phản ứng là phản ứng khử 4-nitrophenol (4-NP) và phản ứng phân hủy phẩm nhuộm methylene lue (MB). Xúc tác Cu/CuFe 2 O 4 có dạng hạt cầu với đường kính trung bình khoảng 145 nm. Kết quả phân tích EDX mapping cho thấy các nguyên tố Cu, Fe và O phân bố đồng đều trong toàn bộ khối cấu trúc vật liệu. Nanocomposite Cu/CuFe 2 O 4 có đặc trưng của vật liệu mao quản trung bình, với diện tích bề mặt BET (S BET ) là 52 m 2 .g -1 . Trong cả hai phản ứng là khử 4-NP và phân hủy MB, vật liệu đều có hoạt tính xúc tác cao. Hiệu suất phản ứng khử 4-NP khi sử dụng xúc tác với sự có mặt của NaBH 4 là 82% sau thời gian 5 phút. Trong phản ứng này, kim loại Cu vừa đóng vai trò là chuyển electron trực tiếp từ ion BH 4 - sang 4-NP vừa tham gia và thúc đẩy quá trình chuyển electron giữa các cặp ion Cu + - Cu 2+ và Fe 2+ -Fe 3+ trong CuFe 2 O 4 . Đối với phản ứng phân hủy MB, hiệu suất phản ứng đạt được là 98% sau thời gian 40 phút, dưới sự kích thích của bức xạ UVA cùng sự có mặt của oxalic acid (H 2 C 2 O 4 ) đóng vai trò tác nhân tạo gốc tự do. Trong quá trình này, Cu là chất cho electron để khử Fe 3+ thành Fe 2+ trong cấu trúc CuFe 2 O 4 , góp phần thúc đẩy sự tạo thành các gốc tự do có hoạt tính cao để phân hủy MB. Hiệu quả xúc tác, cấu trúc tinh thể và hình thái của nanocomposite Cu/CuFe 2 O 4 được duy trì qua năm lần sử dụng liên tiếp nhau trong cả hai phản ứng. Như vậy, xúc tác Cu/CuFe 2 O 4 không chỉ có từ tính tốt để dễ dàng thu hồi mà còn có độ ổn định cao trong điều kiện phản ứng. Đây sẽ là những ưu điểm về mặt kinh tế khi đưa vật liệu ứng dụng vào thực tế.
Lời cảm ơn
Nghiên cứu được tài trợ bởi Đại học Quốc gia Thành phố Hồ Chí Minh (ĐHQG-HCM) trong khuôn khổ Đề tài mã số VL2022-18-04. Nhóm tác giả xin chân thành cám ơn.
DANH MỤC TỪ VIẾT TẮT
BETBrunauer–Emmett–Teller
CAM KẾT XUNG ĐỘT LỢI ÍCH
Nhóm tác giả cam kết không có xung đột lợi ích
ĐÓNG GÓP TÁC GIẢ
Lê Thị Ngọc Hoa, Đặng Tấn Phát, Lê Đặng Thanh An, Đỗ Ngọc Hậu: thực nghiệm
Vũ Năng An, Lê Văn Hiếu: chuẩn bị bản thảo và chỉnh sửa/phản hồi phản biện, hoàn chỉnh bản thảo.
References
- Silva EdN, Brasileiro ILO, Madeira VS, de Farias BA, Ramalho MLA, Rodríguez-Aguado E, et al. Reusable CuFe2O4-Fe2O3 catalyst synthesis and application for the heterogeneous photo-Fenton degradation of methylene blue in visible light. Journal of Environmental Chemical Engineering. 2020;8(5):104132. . ;:. Google Scholar
- Karthik KV, Raghu AV, Reddy KR, Ravishankar R, Sangeeta M, Shetti NP, et al. Green synthesis of Cu-doped ZnO nanoparticles and its application for the photocatalytic degradation of hazardous organic pollutants. Chemosphere. 2022;287:132081. . ;:. PubMed Google Scholar
- Karim Z.. Nanoporous membranes with cellulose nanocrystals as functional entity in chitosan: Removal of dyes from water. Carbohydrate polymers. 2014;112:668-76. . ;:. PubMed Google Scholar
- Krishna R, Fernandes DM, Dias C, Ventura J, Venkata Ramana E, Freire C, et al. Novel synthesis of Ag@Co/RGO nanocomposite and its high catalytic activity towards hydrogenation of 4-nitrophenol to 4-aminophenol. International Journal of Hydrogen Energy. 2015;40(14):4996-5005. . ;:. Google Scholar
- Parmekar MV, Salker AV. Room temperature complete reduction of nitroarenes over a novel Cu/SiO2@NiFe2O4 nano-catalyst in an aqueous medium - a kinetic and mechanistic study. RSC Advances. 2016;6(110):108458-67. . ;:. Google Scholar
- Hasan K, Shehadi IA, Al-Bab ND, Elgamouz A. Magnetic Chitosan-Supported Silver Nanoparticles: A Heterogeneous Catalyst for the Reduction of 4-Nitrophenol. Catalysts. 2019;9(10). . ;:. Google Scholar
- Goyal A, Bansal S, Singhal S. Facile reduction of nitrophenols: Comparative catalytic efficiency of MFe2O4 (M = Ni, Cu, Zn) nano ferrites. International Journal of Hydrogen Energy. 2014;39:4895-908. . ;:. Google Scholar
- Garba ZN, Lawan I, Zhou W, Zhang M, Wang L, Yuan Z. Microcrystalline cellulose (MCC) based materials as emerging adsorbents for the removal of dyes and heavy metals - A review. Science of The Total Environment. 2020;717:135070. . ;:. PubMed Google Scholar
- Chen Y, Wu T, Xing G, Kou Y, Li B, Wang X, et al. Fundamental Formation of Three-Dimensional Fe3O4 Microcrystals and Practical Application in Anchoring Au as Recoverable Catalyst for Effective Reduction of 4-Nitrophenol. Industrial & Engineering Chemistry Research. 2019;58(33):15151-61. . ;:. Google Scholar
- Botsa SM, Kumar YP, Basavaiah K. Facile simultaneous synthesis of tetraaniline nanostructures/silver nanoparticles as heterogeneous catalyst for the efficient catalytic reduction of 4-nitrophenol to 4-aminophenol. RSC Advances. 2020;10(37):22043-53. . ;:. PubMed Google Scholar
- Polat K, Aksu ML, Pekel AT. Electroreduction of nitrobenzene to p-aminophenol using voltammetric and semipilot scale preparative electrolysis techniques. Journal of Applied Electrochemistry. 2002;32(2):217-23. . ;:. Google Scholar
- Taghavi F, Falamaki C, Shabanov A, Bayrami L, Roumianfar A. Kinetic study of the hydrogenation of p-nitrophenol to p-aminophenol over micro-aggregates of nano-Ni2B catalyst particles. Applied Catalysis A: General. 2011;407(1-2):173-80. . ;:. Google Scholar
- Chen R, Wang Q, Du Y, Xing W, Xu N. Effect of initial solution apparent pH on nano-sized nickel catalysts in p-nitrophenol hydrogenation. Chemical Engineering Journal. 2009;145(3):371-6. . ;:. Google Scholar
- Gazi S, Ananthakrishnan R. Metal-free-photocatalytic reduction of 4-nitrophenol by resin-supported dye under the visible irradiation. Applied Catalysis B: Environmental. 2011;105(3-4):317-25. . ;:. Google Scholar
- Ibrahim I, Ali IO, Salama TM, Bahgat A, Mohamed MM. Synthesis of magnetically recyclable spinel ferrite (MFe2O4, M= Zn, Co, Mn) nanocrystals engineered by sol gel-hydrothermal technology: High catalytic performances for nitroarenes reduction. Applied Catalysis B: Environmental. 2016;181:389-402. . ;:. Google Scholar
- Xiong LL, Huang R, Chai HH, Yu L, Li CM. Facile Synthesis of Fe3O4@Tannic Acid@Au Nanocomposites as a Catalyst for 4-Nitrophenol and Methylene Blue Removal. ACS Omega. 2020;5(33):20903-11. . ;:. PubMed Google Scholar
- Zheng H, Huang J, Zhou T, Jiang Y, Jiang Y, Gao M, et al. Recyclable Magnetic Cu/CuFe2O4 Nanocomposites for the Rapid Degradation of 4-NP. Catalysts. 2020;10(12). . ;:. Google Scholar
- Zhang S, Zhao D, Hou C, Liang C, Li H. Facile one-pot synthesis of cellulose nanocrystal-supported hollow CuFe2O4 nanoparticles as efficient catalyst for 4-nitrophenol reduction. Journal of Nanoparticle Research. 2018;20(6):161. . ;:. Google Scholar
- Dey C, De D, Nandi M, Goswami MM. A high performance recyclable magnetic CuFe2O4 nanocatalyst for facile reduction of 4-nitrophenol. Materials Chemistry and Physics. 2020;242:122237. . ;:. Google Scholar
- Sun M, Han X, Chen S. Synthesis and photocatalytic activity of nano-cobalt ferrite catalyst for the photo-degradation various dyes under simulated sunlight irradiation. Materials Science in Semiconductor Processing. 2019;91:367-76. . ;:. Google Scholar
- Guo X, Wang D. Photo-Fenton degradation of methylene blue by synergistic action of oxalic acid and hydrogen peroxide with NiFe2O4 hollow nanospheres catalyst. Journal of Environmental Chemical Engineering. 2019;7(1):102814. . ;:. Google Scholar
- Balcha A, Yadav OP, Dey T. Photocatalytic degradation of methylene blue dye by zinc oxide nanoparticles obtained from precipitation and sol-gel methods. Environmental Science and Pollution Research. 2016;23(24):25485-93. . ;:. PubMed Google Scholar
- Elfeky AS, Salem SS, Elzaref AS, Owda ME, Eladawy HA, Saeed AM, et al. Multifunctional cellulose nanocrystal /metal oxide hybrid, photo-degradation, antibacterial and larvicidal activities. Carbohydrate Polymers. 2020;230:115711. . ;:. PubMed Google Scholar
- Torlopov MA, Martakov IS, Mikhaylov VI, Golubev YA, Sitnikov PA, Udoratina EV. A Fenton-like System (Cu(II)/H2O2) for the Preparation of Cellulose Nanocrystals with a Slightly Modified Surface. Industrial & Engineering Chemistry Research. 2019;58(44):20282-90. . ;:. Google Scholar
- Moncayo-Lasso A, Sanabria J, Pulgarin C, Benítez N. Simultaneous E. coli inactivation and NOM degradation in river water via photo-Fenton process at natural pH in solar CPC reactor. A new way for enhancing solar disinfection of natural water. Chemosphere. 2009;77(2):296-300. . ;:. PubMed Google Scholar
- Nidheesh P. Heterogeneous Fenton catalysts for the abatement of organic pollutants from aqueous solution: a review. Rsc Advances. 2015;5(51):40552-77. . ;:. Google Scholar
- Sahoo B, Sahu SK, Nayak S, Dhara D, Pramanik P. Fabrication of magnetic mesoporous manganese ferrite nanocomposites as efficient catalyst for degradation of dye pollutants. Catalysis Science & Technology. 2012;2(7):1367-74. . ;:. Google Scholar
- Zhang S, Zhao X, Niu H, Shi Y, Cai Y, Jiang G. Superparamagnetic Fe3O4 nanoparticles as catalysts for the catalytic oxidation of phenolic and aniline compounds. Journal of hazardous materials. 2009;167(1-3):560-6. . ;:. PubMed Google Scholar
- Qian X, Ren M, Zhu Y, Yue D, Han Y, Jia J, et al. Visible light assisted heterogeneous Fenton-like degradation of organic pollutant via α-FeOOH/mesoporous carbon composites. Environmental Science & Technology. 2017;51(7):3993-4000. . ;:. PubMed Google Scholar
- Zhang G, Gao Y, Zhang Y, Guo Y. Fe2O3-pillared rectorite as an efficient and stable Fenton-like heterogeneous catalyst for photodegradation of organic contaminants. Environmental science & technology. 2010;44(16):6384-9. . ;:. PubMed Google Scholar
- Gonzalez-Olmos R, Martin MJ, Georgi A, Kopinke F-D, Oller I, Malato S. Fe-zeolites as heterogeneous catalysts in solar Fenton-like reactions at neutral pH. Applied Catalysis B: Environmental. 2012;125:51-8. . ;:. Google Scholar
- Wang Y, Zhao H, Li M, Fan J, Zhao G. Magnetic ordered mesoporous copper ferrite as a heterogeneous Fenton catalyst for the degradation of imidacloprid. Applied Catalysis B: Environmental. 2014;147:534-45. . ;:. Google Scholar
- Li Y, Shen J, Hu Y, Qiu S, Min G, Song Z, et al. General flame approach to chainlike MFe2O4 spinel (M= Cu, Ni, Co, Zn) nanoaggregates for reduction of nitroaromatic compounds. Industrial & Engineering Chemistry Research. 2015;54(40):9750-7. . ;:. Google Scholar
- Zhao Y, He G, Dai W, Chen H. High catalytic activity in the phenol hydroxylation of magnetically separable CuFe2O4-reduced graphene oxide. Industrial & Engineering Chemistry Research. 2014;53(32):12566-74. . ;:. Google Scholar
- Qin Q, Liu Y, Li X, Sun T, Xu Y. Enhanced heterogeneous Fenton-like degradation of methylene blue by reduced CuFe 2 O 4. RSC advances. 2018;8(2):1071-7. . ;:. PubMed Google Scholar
- Wang Y, Zhao H, Zhao G. Iron-copper bimetallic nanoparticles embedded within ordered mesoporous carbon as effective and stable heterogeneous Fenton catalyst for the degradation of organic contaminants. Applied Catalysis B: Environmental. 2015;164:396-406. . ;:. Google Scholar
- Zhou P, Zhang J, Zhang Y, Liang J, Liu Y, Liu B, et al. Activation of hydrogen peroxide during the corrosion of nanoscale zero valent copper in acidic solution. Journal of Molecular Catalysis A: Chemical. 2016;424:115-20. . ;:. Google Scholar
- Ma X, Cheng Y, Ge Y, Wu H, Li Q, Gao N, et al. Ultrasound-enhanced nanosized zero-valent copper activation of hydrogen peroxide for the degradation of norfloxacin. Ultrasonics sonochemistry. 2018;40:763-72. . ;:. PubMed Google Scholar
- Wen G, Wang S-J, Ma J, Huang T-L, Liu Z-Q, Zhao L, et al. Oxidative degradation of organic pollutants in aqueous solution using zero valent copper under aerobic atmosphere condition. Journal of Hazardous Materials. 2014;275:193-9. . ;:. PubMed Google Scholar
- Gao Q, Sun Z. Facile fabrication of uniform MFe2O4 (M= Co, Ni, Cu) hollow spheres and their recyclable superior catalytic activity towards 4-nitrophenol reduction. Journal of Nanoscience and Nanotechnology. 2018;18(8):5645-53. . ;:. PubMed Google Scholar
- Li X, Liu A, Chu D, Zhang C, Du Y, Huang J, et al. High performance of manganese porphyrin sensitized p-type CuFe2O4 photocathode for solar water splitting to produce hydrogen in a tandem photoelectrochemical cell. Catalysts. 2018;8(3):108. . ;:. Google Scholar
- Goyal A, Bansal S, Singhal S. Facile reduction of nitrophenols: Comparative catalytic efficiency of MFe2O4 (M= Ni, Cu, Zn) nano ferrites. International journal of hydrogen energy. 2014;39(10):4895-908. . ;:. Google Scholar
- Hou C, Zhao D, Chen W, Li H, Zhang S, Liang C. Covalent organic framework-functionalized magnetic CuFe2O4/Ag nanoparticles for the reduction of 4-nitrophenol. Nanomaterials. 2020;10(3):426. . ;:. PubMed Google Scholar
- Frusteri L, Cannilla C, Todaro S, Frusteri F, Bonura G. Tailoring of Hydrotalcite-derived Cu-based catalysts for CO2 hydrogenation to methanol. Catalysts. 2019;9(12):1058. . ;:. Google Scholar
- Gao J, Gao S, Wei J, Zhao H, Zhang J. Catalytic combustion of dimethyl disulfide on bimetallic supported catalysts prepared by the wet-impregnation method. Catalysts. 2019;9(12):994. . ;:. Google Scholar
- Li Z, Lyu J, Ge M. Synthesis of magnetic Cu/CuFe2O4 nanocomposite as a highly efficient Fenton-like catalyst for methylene blue degradation. Journal of Materials Science. 2018;53(21):15081-95. . ;:. Google Scholar
- Koley P, Chandra Shit S, Joseph B, Pollastri S, Sabri YM, Mayes EL, et al. Leveraging Cu/CuFe2O4-catalyzed biomass-derived furfural hydrodeoxygenation: a nanoscale metal-organic-framework template is the prime key. ACS applied materials & interfaces. 2020;12(19):21682-700. . ;:. PubMed Google Scholar
- Zhang S, Zhao D, Hou C, Liang C, Li H. Facile one-pot synthesis of cellulose nanocrystal-supported hollow CuFe 2 O 4 nanoparticles as efficient catalyst for 4-nitrophenol reduction. Journal of Nanoparticle Research. 2018;20(6):161. . ;:. Google Scholar
- Liu W-J, Tian K, Jiang H, Yu H-Q. Harvest of Cu NP anchored magnetic carbon materials from Fe/Cu preloaded biomass: their pyrolysis, characterization, and catalytic activity on aqueous reduction of 4-nitrophenol. Green Chemistry. 2014;16(9):4198-205. . ;:. Google Scholar
- Deka P, Deka RC, Bharali P. In situ generated copper nanoparticle catalyzed reduction of 4-nitrophenol. New Journal of Chemistry. 2014;38(4):1789-93. . ;:. Google Scholar
- Bai Y, Wang Q, Du C, Bu T, Liu Y, Sun X, et al. Three-dimensional Cu/C porous composite: Facile fabrication and efficient catalytic reduction of 4-nitrophenol. Journal of Colloid and Interface Science. 2019;553:768-77. . ;:. PubMed Google Scholar
- Kang X, Teng D, Wu S, Tian Z, Liu J, Li P, et al. Ultrafine copper nanoparticles anchored on reduced graphene oxide present excellent catalytic performance toward 4-nitrophenol reduction. Journal of Colloid and Interface Science. 2020;566:265-70. . ;:. PubMed Google Scholar
- Oulego P, Villa-García MA, Laca A, Diaz M. The effect of the synthetic route on the structural, textural, morphological and catalytic properties of iron(III) oxides and oxyhydroxides. Dalton Transactions. 2016;45(23):9446-59. . ;:. PubMed Google Scholar
- Zhang X, Feng M, Qu R, Liu H, Wang L, Wang Z. Catalytic degradation of diethyl phthalate in aqueous solution by persulfate activated with nano-scaled magnetic CuFe2O4/MWCNTs. Chemical engineering journal. 2016;301:1-11. . ;:. Google Scholar
- Tian C, Fu S, Lucia LA. Magnetic Cu 0.5 Co 0.5 Fe 2 O 4 ferrite nanoparticles immobilized in situ on the surfaces of cellulose nanocrystals. Cellulose. 2015;22(4):2571-87. . ;:. Google Scholar
- Parhizkar J, Habibi MH, Mosavian SY. Synthesis and Characterization of Nano CoFe2O4 Prepared by Sol-Gel Auto-Combustion with Ultrasonic Irradiation and Evaluation of Photocatalytic Removal and Degradation Kinetic of Reactive Red 195. Silicon. 2019;11(2):1119-29. . ;:. Google Scholar
- Gangula A, Podila R, M R, Karanam L, Janardhana C, Rao AM. Catalytic Reduction of 4-Nitrophenol using Biogenic Gold and Silver Nanoparticles Derived from Breynia rhamnoides. Langmuir. 2011;27(24):15268-74. . ;:. PubMed Google Scholar
- Guo Y, Zhang L, Liu X, Li B, Tang D, Liu W, et al. Synthesis of magnetic core-shell carbon dot@MFe2O4 (M = Mn, Zn and Cu) hybrid materials and their catalytic properties. Journal of Materials Chemistry A. 2016;4(11):4044-55. . ;:. Google Scholar
- Hao P, Hu M, Xing R, Zhou W. Synergistic degradation of methylparaben on CuFe2O4-rGO composite by persulfate activation. Journal of Alloys and Compounds. 2020;823:153757. . ;:. Google Scholar
- Wissmeyer G, Pleitez MA, Rosenthal A, Ntziachristos V. Looking at sound: optoacoustics with all-optical ultrasound detection. Light: Science & Applications. 2018;7(1):53. . ;:. PubMed Google Scholar
- Mulazzani QG, D'Angelantonio M, Venturi M, Hoffman MZ, Rodgers MA. Interaction of formate and oxalate ions with radiation-generated radicals in aqueous solution. Methylviologen as a mechanistic probe. The Journal of Physical Chemistry. 1986;90(21):5347-52. . ;:. Google Scholar
- Liu S-Q, Feng L-R, Xu N, Chen Z-G, Wang X-M. Magnetic nickel ferrite as a heterogeneous photo-Fenton catalyst for the degradation of rhodamine B in the presence of oxalic acid. Chemical Engineering Journal. 2012;203:432-9. . ;:. Google Scholar
- Wang Y, Li J, Sun J, Wang Y, Zhao X. Electrospun flexible self-standing Cu-Al 2 O 3 fibrous membranes as Fenton catalysts for bisphenol A degradation. Journal of Materials Chemistry A. 2017;5(36):19151-8. . ;:. Google Scholar
- Ge M, Li Y, Liu L, Zhou Z, Chen W. Bi2O3− Bi2WO6 composite microspheres: hydrothermal synthesis and photocatalytic performances. The Journal of Physical Chemistry C. 2011;115(13):5220-5. . ;:. Google Scholar

 Open Access
Open Access