Abstract
Ngoc Linh ginseng or Vietnamese ginseng (Panax vietnamensis Ha et Grushv.) of the Araliaceae family, a endemic plant in Ngoc Linh mountain, is the 20th type of ginseng found in the world (1985). The content of saponin of Ngoc Linh ginseng is much higher than that of other ginsengs in the world such as Panax ginseng (Korean ginseng), anax quinquefolium(American ginseng) and anax notoginseng (Chinese ginseng). Until now, from roots, rhizomes and leaves of Ngoc Linh ginseng, there are 63 saponin which were isolated and determined structures. In addition, polyacetylenes, polyphenols, fatty alcohols and amino acids were also reported. Some of them showed diverse biological activities. In this research, from Ngoc Linh ginseng leaves, six compounds were isolated and structural elucidated by 1D and 2D NMR, MS spectroscopic methods and comparison of the spectral data with those in literature. They were one triterpene, squalene (1), one quinone terpenoid, a-tocopherolquinone (2), two fatty alcohols, tetradecanol (3), docosanol (4) from the -hexane extract and a steroid glycoside, daucosterol (5) and one flavonoid, kaempferol (6) from the methanol extract. All six compounds were reported for the first time from Ngoc Linh ginseng leaves.
MỞ ĐẦU
Sâm Ngọc Linh hay còn gọi tên khác là sâm Việt Nam, sâm Khu 5, cây Thuốc giấu…, có tên khoa học là Panax vietnamensis Ha et Grushv. (Hà Thị Dụng và Grushvisky, 1985), thuộc họ Nhân Sâm (Araliaceae) 1 . Sâm Ngọc Linh là loài cây thân thảo lâu năm, được phân bố chủ yếu vùng núi Ngọc Linh, thuộc hai tỉnh Quảng Nam và Kon Tum của Việt Nam 2 , 3 , 4 . Thân rễ và củ sâm được sử dụng làm thuốc chữa bệnh, còn lá và thân thì được dùng làm trà sâm. Trong dân gian, sâm Ngọc Linh được dùng trong các trường hợp bệnh thông thường, bệnh nặng hay dùng để bồi dưỡng cơ thể 4 . Các nghiên cứu trước đây về thành phần hóa học của sâm Ngọc Linh đã cho biết thành phần hóa học chủ yếu là saponin thuộc hai khung là dammarane và oleanane 5 , và các hợp chất khác như polyacetylene, acid béo hay daucosterol 6 . Nội dung bài báo trình bày về việc phân lập sáu hợp chất từ lá sâm Ngọc Linh [squalene (1) , α -tocopherolquinone (2) , tetradecanol (3), docosanol (4) , daucosterol ( 5 ) và kaempferol (6) ]. Cấu trúc hóa học các hợp chất này được xác định bằng các phương pháp phân tích phổ nghiệm.
PHƯƠNG PHÁP THỰC NGHIỆM
Hóa chất và thiết bị
Dung môi hữu cơ sử dụng trong sắc ký cột và sắc ký lớp mỏng: n -hexane, chloroform, ethyl acetate, methanol, acetone đều là hóa chất của hãng Chemsol–Việt Nam. Sắc ký lớp mỏng (TLC) được thực hiện trên silica gel 60 F 254 hoặc silica gel 60 RP-18 F 254 S (Merck). Thuốc thử hiện màu: dung dịch H 2 SO 4 10%; dung dịch 5% vanillin/ethanol. Silica gel sắc ký cột pha thường sử dụng silica gel 230-400 mesh RM7484, pha đảo sử dụng silica gel RP-18 (25-40µm).
Các thiết bị ghi phổ tại Phòng Phân tích Trung tâm, Trường Đại học Khoa học Tự nhiên, Đại học Quốc gia TP. Hồ Chí Minh: phổ 1D và 2D NMR được ghi trên máy cộng hưởng từ hạt nhân Bruker Avance 500, 500 MHz cho phổ 1 H NMR và 125 MHz cho phổ 13 C NMR. Khối phổ ESI-HR MS được ghi máy Agilent 1100 series.
Quá trình thực nghiệm
Nguyên liệu lá sâm Ngọc Linh được cung cấp bởi Công ty TNHH MTV Lâm Nghiệp Đắk Tô vào tháng 10/2019. Lá sâm sau khi phơi khô, xác định độ ẩm, được xay thành dạng bột và thực hiện chiết bằng cách đun hoàn lưu với các đơn dung môi theo thứ tự độ phân cực tăng dần: n -hexane, chloroform, ethyl acetate và methanol. Mỗi đơn dung môi được thực hiện chiết 4 lần. Bình chiết thể tích 5 L chứa 500 g nguyên liệu lá sâm khô đã xay nhỏ, 2,5 L dung môi, đun hoàn lưu 3 tiếng/lần. Tổng khối lượng nguyên liệu lá sâm Ngọc Linh khô là 3957 g. Lọc lấy dung dịch, cô quay thu hồi dung môi dưới áp suất kém, thu được cao chiết tương ứng. Khối lượng các cao thu được gồm bốn loại cao: n- hexane (97,50 g cao HE), chloroform (62,23 g cao CL), ethyl acetate (102,85 g cao EA) và methanol (853,02 g cao ME).
Cao HE được sắc ký cột silica gel pha thường, giải ly với n -hexane:chloroform (100:0; 95:5; 90:10; 50: 50; 0:100), thu được 6 phân đoạn (HE1-HE6). Phân đoạn HE2 (120,0 mg) tiếp tục được triển khai sắc ký cột silica gel pha thường thu được 3 phân đoạn (HE2.1-HE2.3). Sắc ký lớp mỏng điều chế đối với phân đoạn HE2.1 (20,3 mg) với dung môi giải ly n -hexane 100%, thu được hợp chất 1 (9,0 mg). Phân đoạn HE3 (5,19 g) được sắc ký cột silica gel pha thường với quy trình tương tự như cho phân đoạn HE2, thu được 27 phân đoạn (HE3.1-HE3.27). Sắc ký cột silica gel pha thường với hệ dung môi giải ly n -hexane:choloroform (99:1) đối với 2 phân đoạn HE3.14.15 (35,3 mg) và HE3.14.20 (25,6 mg), thu được lần lượt hợp chất 2 (13,6 mg) và 3 (7,5 mg). Phân đoạn HE4 (15,70 g) được thực hiện sắc ký cột tương tự HE2 và HE3 thu được 14 phân đoạn (HE4.1-HE4.14). Sắc ký cột silica gel pha thường với hệ dung môi giải ly n -hexane:chloroform (99:1) trên phân đoạn HE4.14 (1,27 g) thu được hợp chất 4 (10,3 mg).
Cao ME (853,50 g) được chiết rắn-lỏng lần lượt với các hệ ethyl acetate:methanol (100:0; 90:10; 80:20; 70:30; 60:40) thu được 5 cao (ME1-ME5). Cao ME2 được sắc ký cột silica gel pha thường, giải ly với ethyl acetate:methanol (98:2; 95:5; 90:10; 80:20; …; 0:100) thu được 4 phân đoạn (ME2.1-ME2.4). Phân đoạn ME2.2 (440,0 mg) được sắc ký cột silica gel pha thường, giải ly với ethyl acetate:methanol (98:2; 95:5; 90:10; 80:20; …; 0:100) thu được 9 phân đoạn (ME2.2.1-M2.2.9). Phân đoạn ME2.2.2 (32,7 mg) được sắc ký cột silica gel pha đảo với hệ dung môi giải ly methanol:nước (9:1) thu được hợp chất 5 (5,3 mg). Cao ME5 (125,22 g) được sắc ký cột silica gel pha thường, giải ly ethyl acetate:methanol (90:10; 80:20;…; 0:100) thu được 8 phân đoạn (ME5.1-ME5.8). Chiết lỏng-lỏng trên phân đoạn ME5.4 (2,56 g) với dung môi chloroform và nước thu được phần cao chiết chloroform ME5.4.1 (218,0 mg) và cao chiết nước ME5.4.2 (2,13 g). Cao ME5.4.1 được sắc ký cột silica gel pha thường với hệ dung ly chloroform:methanol, được 6 phân đoạn (ME5.4.1.1-ME5.4.1.6). Phân đoạn ME5.4.1.3 (15,2 mg) được sắc ký cột với chloroform:methanol (90:10) thu được hợp chất 6 (6,8 mg).
KẾT QUẢ
Từ cao n -hexane và cao methanol của lá sâm Ngọc Linh ( Panax vietnamensis ) đã phân lập được sáu hợp chất, bao gồm: squalene (1) , α -tocopherolquinone (2) , tetradecanol (3) , docosanol (4) , daucosterol ( 5 ), kaempferol (6 ) ( Figure 1 ).
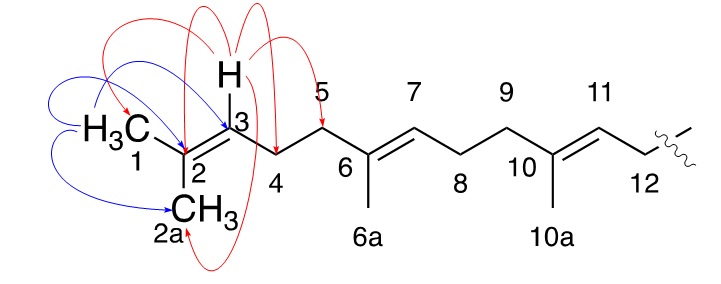
Squalene (1): có dạng dầu màu vàng nhạt (ESI-HR MS: m/ 433,3819 [C 30 H 50 +Na] + (ΔM= 0,8 mmass). CTPT: C 30 H 50 . 1 H NMR (CDCl 3 , δ H ppm, J Hz): 5,14 (1H, d, 7,6, H-11); 5,12 (1H, m, H-7); 5,09 (1H, m, H-3); 2,08 (4H, m, H-4 và H-8); 2,00 (6H, m, H-5, H-9 và H-12); 1,68 (3H, s, H-1); 1,60 (9H, s , H-2a, H-6a và H-10a). 13 C NMR (CDCl 3 , δ C ppm): 25,8 (C-1); 131,4 (C-2); 124,6 (C-3); 27,0 (C-4); 39,9 (C-5 và C-8); 135,1 (C-6); 124,5 (C-7); 26,9 (C-9); 135,3 (C-10); 124,5 (C-11); 28,5 (C-12); 17,8 (C-2a); 16,2 (C-6a); 16,1 (C-10a).
α -Tocopherolquinone (2): dạng dầu màu vàng, +45 ( c 0.05, CHCl 3 ). 1 H NMR (CDCl 3 , δ H ppm, J Hz): 2,54 (2H, m , H-4); 2,03 (3H, s , H-5a); 2,00 (6H, s , H-7a, H-8a); 1,23 (3H, s , H-2a); 0,86 (9H, d , 6,8, H-4a’, H-8a’, H-12a’); 0,84 (3H, d , 6,6, H-13’); 1,00–1,65 (CH và CH 2 bão hòa). 13 C NMR (CDCl 3 , δ C ppm): 72,8 (C-2); 40,5(C-3); 21,5 (C–4); 140,6 (C-5); 187,8 (C-6); 140,3 (C-7); 140,7 (C-8); 187,4 (C-9); 144,6 (C-10); 22,8 (C-2a); 12,1 (C-5a); 12,4 (C-7a); 12,5 (C-8a); 19,9 (C-4a’); 42,5 (C-1’); 21,6 (C-2’); 37,8 (C-3’); 33,0 (C-4’, C-8’); 37,6 (C-5’); 24,7 (C-6’); 37,6 (C-7’); 37,5 (C-9’); 25,0 (C-10’); 39,6 (C-11’); 28,1 (C-12’); 22,8 (C-12’).
Tetradecanol ( 3) : dạng sáp màu trắng, vô định hình (ESI-HR MS: m /z 197,2258 [C 14 H 29 –OH] + (ΔM= 1,1 mmass). CTPT: C 14 H 30 O. 1 H NMR (CDCl 3 , δ H ppm, J Hz): 4,05 (2H, H-1); 2,04 (2H, H-2) và 1,64 (2H, H-3); 1,26 (20H, H-4 đến H-13); 0,88 (3H, t , 6,91, H-14). 13 C NMR (CDCl 3 , δ C ppm): 14,2 (C-14); 64,8 (C-1); 32,1 (C-2); 21,1 (C-13); C-3 đến C-12: 29,9; 29,9; 29,8; 29,7; 29,7; 29,5; 29,4; 28,8; 26,1; 22,8.
Docosanol (4) : dạng sáp màu trắng, vô định hình. ESI-MS: m/z 326,43 [C 22 H 45 OH] – . CTPT: C 22 H 46 O. 1 H NMR (CDCl 3 , δ H ppm, J Hz): 3,64 (2H, t , 6,6, H-1); 1,26 (36H, m , H-2 đến H-21); 0,88 (3H, t , 6,9, H-22). 13 C NMR (CDCl 3 , δ C ppm): 63,1 (C-1); 14,3 (C-22); 33,0 (C-2); 22,9 (C-21); C-3 đến C-20: 33,0; 32,1; 29,9; 29,8; 29,8; 29,8; 29,6; 29,5; 25,9; 22,9.
Daucosterol ( 5 ): Hợp chất dạng bột, màu trắng. 1 H NMR (pyridine– d 5 , δ H ppm, J Hz): 5,38 (1H, m , H-6); 5,07 (1H, d , 7,8, H–1’); 4,59 (1H, d , 11,4, H-6’b); 4,42 (1H, dd , 11,7, 5,2, H-6’a); 4,30 (1H, t , 7,0, H-3’); 4,30 (1H, m , H-4’); 4,07 (1H, t , 8,0, H-2’); 4,01 (1H, m , H-3); 3,98 (1H, m , H-5’); 1,00 (3H, d , 6,4, H-21); 0,95 (3H, s , H-19); 0,91 (3H, m , H-29); 0,90 (3H, d , 5,0, H–27); 0,87 (3H, d , 6,9, H-26); 0,67 (3H, s , H-18). 13 C NMR (pyridine- d 5 , δ C ppm): 141,5 (C-5); 122,4 (C-6); 103,1 (C-1’); 79,1 (C-3); 79,0 (C-3’); 78,7 (C-5’); 75,9 (C-2’); 72,3 (C-4’); 63,4 (C-6’); 57,4 (C-14); 56,8 (C-17); 50,9 (C-9); 46,6 (C-24); 43,0 (C-13); 40,5 (C-12); 39,9 (C-4); 38,0 (C-1); 37,5 (C-10); 36,9 (C-20); 34,8 (C-22); 32,7 (C–7); 32,6 (C-8); 30,8 (C-2); 30,0 (C-25); 29,1 (C-16); 27,0 (C-23); 25,0 (C-15); 23,9 (C-28); 21,8 (C-11); 20,5 (C-27); 19,9 (C-19); 19,7 (C–26); 19,5 (C-21); 12,7 (C-18); 12,5 (C-29).
Kaempferol (6) : hợp chất dạng bột màu vàng. 1 H NMR (CDCl 3 , δ H ppm, J Hz): 8,14 (2H, d , 8,9, H-2’ và H-6’); 6,95 (2H, d , 8,9, H-3’ và H-5’); 6,44 (1H, d , 2,1, H-8); 6,23 (1H, d , 2,1, H-6). 13 C NMR (CDCl 3 , δ C ppm): 176,1 (C-4); 164,2 (C-7); 161,1 (C-5); 159,14 (C-9); 156,9 (C-4’); 146,7 (C-2); 135,8 (C-3); 129,3 (C-2’ và C-6’); 122,4 (C-1’); 114,9 (C-3’ và C-5’), 103,2 (C-10); 97,9 (C-6); 93,1 (C-8).
THẢO LUẬN
Phổ 1 H NMR của hợp chất 1 cho tín hiệu của 25 proton, phổ 13 C NMR cho 15 tín hiệu carbon và khối phổ ESI-HR MS cho mũi ion phân tử giả m/z 433,3819 [C 30 H 50 +Na] + (ΔM = 0,8 mmass), tương ứng với CTPT C 30 H 50 . Các dữ kiện trên giúp suy đoán 1 là một triterpene có cấu trúc đối xứng và tín hiệu NMR thể hiện cho mảnh của ½ phân tử. Trong vùng δ C 120–140 có sáu tín hiệu carbon olefin. Trên phổ HSQC cho thấy tương quan proton và carbon của ba trong số sáu carbon này với ba proton vùng δ H 5,11, vậy 1 có thể có sáu nối đôi C=C. Trong vùng δ H 1,60–1,70 có bốn tín hiệu của bốn nhóm methyl gắn trực tiếp với carbon olefin, vậy 1 có thể có 8 nhóm methyl. Ngoài ra còn 10 tín hiệu proton của các nhóm methylene ở δ H 2,00–2,10 gắn với các carbon có δ C 25,0–40,0. Phổ HMBC ( Figure 2 ) cho các tín hiệu tương quan giữa H-1 với C-2, C-2a và C3; tương quan giữa H-3 với C-1, C-2, C-2a, C-3, C-4 và C-5; tương tự cho các proton bên cạnh. So sánh dữ liệu phổ của hợp chất 1 với tài liệu tham khảo 7 cho thấy hợp chất 1 là squalene.
Phổ 1 H NMR của hợp chất 2 có năm tín hiệu proton mũi đơn, nhóm methyl δ H 2,03 (3H, s , H-5a); 2,00 (6H, s , H-7a, H-8a); 1,23 (3H, s , H-2a); 0,86 (9H, d , 6,8 Hz, H-4a’, H-8a’, H-12a’); 0,84 (3H, d , 6,6 Hz, H-13’), một tín hiệu proton methine mũi đa tại δ H 2,54 (2H, m , H-4). Các tín hiệu của methine và methylene còn lại tại vùng 1,00-1,65 ppm. Phổ 13 C NMR của 2 cho 28 tín hiệu carbon. Trong đó, có 2 tín hiệu carbon carbonyl δ C 187,6 (C-6) và 187,2 (C-9), bốn tín hiệu carbon thơm tại δ C 140,0 –145,0; một tín hiệu carbon tứ cấp gắn oxygen tại δ C 72,7 (C-2). Còn lại 21 tín hiệu carbon sp 3 cộng hưởng ở vùng từ trường cao. So sánh dữ liệu phổ của hợp chất 2 với tài liệu tham khảo 8 có thể đề nghị 2 là α -tocopherolquinone.
Phổ 1 H NMR NMR 3 cho thấy một tín hiệu proton methyl đầu mạch δ H 0,88 (3H, t , 6,9 Hz). Một tín hiệu proton oxymethylene δ H 4,05 (2H, H-1) và các tín hiệu proton sp 3 còn lại cộng hưởng ở vùng từ trường cao δ H 1,20–2,10. Phổ 13 C NMR cho 12 tín hiệu, trong đó có một tín hiệu carbon methyl δ C 14,2 (C-14), một tín hiệu carbon oxymethylene δ C 64,8 (C-1), còn lại là các tín hiệu carbon sp 3 dây béo ở vùng δ C 20,0-32,0. Khối phổ ESI-HR MS cho mũi ion phân tử giả m/z =197,2258 [C 14 H 28 –H 2 O] + (ΔM = 1,1 mmass), tương ứng CTPT: C 14 H 30 O. So sánh dữ liệu phổ với tài liệu tham khảo 9 có thể kết luận hợp chất 3 là tetradecanol.
Phổ 1 H NMR của hợp chất 4 cho thấy một tín hiệu nhóm methyl đầu mạch tại δ H 0,88 (3H, t , 6,9 Hz, H-22), một tín hiệu oxymethylene tại δ H 3,64 (2H, t , 6,6 Hz, H-1) và các tín hiệu proton gắn trên carbon sp 3 còn lại trong vùng δ H 1,20–1,30. Phổ 13 C NMR cho một tín hiệu carbon gắn với dị nguyên tố tại δ C 63,1 (C-1), một tín hiệu carbon nhóm methyl đầu mạch tại δ C 14,3 (C-22), còn lại là các tín hiệu carbon sp 3 dây béo tại δ C 22,0-33,0. Khối phổ ESI MS cho mũi ion phân tử giả m/z 326,43 [C 22 H 45 OH] – tương ứng với CTPT: C 22 H 46 O. Vậy đề nghị hợp chất 4 là docosanol.
Phổ 1 H NMR của hợp chất 5 cho sáu tín hiệu nhóm methyl δ H 1,00 (3H, d , 6,4, H-21); 0,95 (3H, s , H-19); 0,91 (3H, m , H-29); 0,90 (3H, d , 5,0 Hz, H-27); 0,87 (3H, d , 6,9 Hz, H-26) và 0,67 (3H, s , H-18). Các tín hiệu phổ đặc trưng của đường -glucose: δ H 5,07 (1H, d , 7,8 Hz, H-1’, proton anomer); 4,59 (1H, d , 11,4 Hz, H-6’b); 4,42 (1H, dd , 11,7, 5.2 Hz, H-6’a); 4,30 (1H, t , 7,0 Hz, H-3’); 4,30 (1H, m , H-4’); 4,07 (1H, t , 8,0 Hz, H-2’) và 3,98 (1H, m , H–5’). Tín hiệu proton cộng hưởng ở vùng từ trường thấp còn lại là của C-3 vòng aglycon gắn đường tại δ H 4,01 (1H, m , H-3). Phổ 13 C NMR cho 35 tín hiệu carbon. Trong đó, phần aglycon có sáu tín hiệu carbon nhóm methyl tại δ C 20,5 (C-27); 19,9 (C-19); 19,7 (C-26); 19,5 (C-21); 12,7 (C-18); 12,5 (C-29), hai tín hiệu carbon olefin tại δ C 141,5 (C-5); 122,4 (C-6), một tín hiệu đặc trưng của carbon trên khung aglycon gắn với đường tại δ C 79,1 (C-3), còn lại 20 tín hiệu carbon nhóm methylene và methine của aglycon ở δ C 20,0–56,0. Phần đường -glucose gồm sáu tín hiệu tại δ C : 103,1 (C-1’); 79,0 (C-3’); 78,7 (C-5’); 75,9 (C-2’); 72,3 (C-4’); 63,4 (C-6’). Sự tương đồng về dữ liệu phổ NMR của 5 với tài liệu tham khảo 10 cho thấy đây là daucosterol.
Phổ 1 H NMR của hợp chất 6 cho bốn tín hiệu proton mũi đôi của sáu proton thơm, trong đó hai tín hiệu proton vòng C tại vị trí ortho với nhau là δ H 8,14 (2H, d , 8,9 Hz, H-2’, 6’); 6,95 (2H, d , 8,9 Hz, H-3’,5’) và hai tín hiệu proton vòng A tại vị trí meta với nhau là δ H 6,44 (1H, d , 2,1 Hz, H-8); 6,23 (1H, d , 2,1 Hz , H-6). Phổ 13 C NMR của hợp chất 6 cho 13 tín hiệu carbon trong đó có một tín hiệu carbon carbonyl tại δ C 176,1; bảy tín hiệu carbon thơm tứ cấp tại δ C 103,0–165,0; một carbon oxyolefin tứ cấp δ C 135,8; bốn tín hiệu carbon methine thơm ở δ C 90,0–130,0. Kết hợp với tài liệu tham khảo 11 cho thấy cấu trúc hợp chất 6 là kaempferol.
KẾT LUẬN
Nghiên cứu thành phần hóa học của cao n -hexane và methanol lá sâm Ngọc Linh bằng các kỹ thuật sắc ký cột kết hợp với sắc ký lớp mỏng điều chế đã phân lập được sáu hợp chất tinh sạch. Trên cơ sở phổ NMR và MS kết hợp với so sánh tài liệu tham khảo, các hợp chất được xác định là: squalene (1) , α -tocopherolquinone (2) , tetradecanol (3) , docosanol (4) , daucosterol ( 5 ) và kaempferol (6). Tất cả sáu hợp chất lần đầu tiên được biết đến với sự hiện diện trong lá sâm Ngọc Linh ( Panax vietnamensis ).
LỜI CẢM ƠN
Nghiên cứu này được tài trợ bởi Sở Khoa học và Công nghệ tỉnh Kon Tum, trong khuôn khổ đề tài mã số 04/2019/ HĐ-KHCN, được thực hiện ở Phòng thí nghiệm Hóa Hữu cơ, Đại học Khoa học Tự nhiên, 227 Nguyễn Văn Cừ, phường 4, quận 5, thành phố Hồ Chí Minh.
DANH MỤC CÁC TỪ VIẾT TẮT
HR-ESI-MS : High resolution- Electrospray ionization-Mass spectrometry
1 H NMR : Proton nuclear magnetic resonance
13 C NMR : Carbon-13 nuclear magnetic resonance
HSQC : Heteronuclear Single Quantum Correlation Spectroscopy
HMBC : Heteronuclear multiple bond correlation
s : singlet
d : doublet
t : triplet
m : multiplet
XUNG ĐỘT LỢI ÍCH
Nhóm tác giả cam kết không có xung đột lợi ích khi thực hiện nghiên cứu này.
ĐÓNG GÓP CỦA CÁC TÁC GIẢ
Tất cả tác giả đều tham gia, đóng góp vào việc tư vấn, thiết kế quy trình thí nghiệm, thực hiện thí nghiệm; tổng hợp và xử lý các kết quả, dữ liệu thu được từ các phương pháp phổ nghiệm (NMR và MS).
Thực hiện viết bản thảo: Lê Hoàng Khang, Phan Thanh Tùng.
Tôn Thất Quang chỉnh sửa, hoàn chỉnh và duyệt bản thảo cuối với sự đồng thuận của tất cả các tác giả.
References
- Dung HT, Grushvisky IV. A new species of the genus Panax L., Araliaceae in Vietnam: Panax vietnamensis Ha et Grushv, Bot. J. Vietnam, 1985, 70, 518-522. . ;:. Google Scholar
- Nguyễn TD. Sâm Việt Nam và một số cây thuốc họ Nhân Sâm, Nhà xuất bản Khoa học Kỹ thuật Hà Nội, 2007, 69-78. . ;:. Google Scholar
- Đỗ TL. Cây thuốc và vị thuốc Việt Nam, Nhà xuất bản Khoa học và Kỹ thuật, 1995, 808. . ;:. Google Scholar
- Võ VC. Từ điển Cây thuốc Việt Nam, Tập 2, Nhà xuất bản Y học; 1997, 674. . ;:. Google Scholar
- Nguyen MD, Nguyen TN, Ryoji K, Aiko I, Kazuo Y và Osamu T. Saponins from Vietnamese ginseng, Panax vietnamensis Ha et Grushv. Collected in central Vietnam. I, Chem. Pharm. Bull., 41, 1993, 2010-2014. . ;:. PubMed Google Scholar
- Lutomski J, Tran CL, Hoa TT. Polyacetylenes in the Araliaceae family. Part IV. The antibacterial and antifungal activities of two main polyacetylenes from Panax vietnamensis Ha et Grushv. and Polyscias fruticosa (L.) Harms, Herba Polonica, 1992, 38, 137-140. . ;:. Google Scholar
- Lionello P, Maurizio C, Gabriele R, Davide V. An NMR and molecular mechanics study of squalene and squalene derivatives, Chemistry and Physics of Lipids, 1994, 70, 21-34. . ;:. Google Scholar
- Cho J. G.. Acyclic diterpenoids from the leaves of Capsicum annuum, J. Appl. Biol Chem., 2009, 52, 128-132. . ;:. Google Scholar
- Sjövold H. Solvent-Free Synthesis of Glycidyl Ethers. Investigating Factors Influencing the yield of alkyl glycidyl ethers. Master's thesis, Chalmers University of Technology, Sweden. . 2015;:. Google Scholar
- Torres-Ortiz DA, Rodríguez-deLeón E, Bah M. Vasorelaxing effect and possible chemical markers of the flowers of the Mexican Crataegus gracilior, Supplementary Material, 2019, 1-25. . ;:. Google Scholar
- Cong N., T.Tram Kaempferol and kaempferol glycosides from Phyllanthies acidus leaves, Vietnam Journal of Chemistry, 2016, 54, 6, 790-793. . ;:. Google Scholar

 Open Access
Open Access